
Résumés CPLF 2026
Association entre la FeNO à l’inclusion et l’évolution du mucus chez les patients atteints d'asthme modéré à sévère non contrôlé traités par dupilumab dans l’étude VESTIGE
Auteur correspondant : Yeboah S.
Introduction
Le dupilumab est un anticorps monoclonal entièrement humain qui bloque la signalisation de l’interleukine IL-4 et de l’IL-13, des médiateurs clés et centraux de l’inflammation de type 2. Dans l’étude VESTIGE (NCT04400318), l’imagerie fonctionnelle respiratoire a montré que le traitement par dupilumab réduisait significativement le score et le volume de mucus chez des patients atteints d’asthme modéré à sévère présentant des biomarqueurs élevés d’inflammation de type 2. Cette analyse post hoc a été menée afin de déterminer si la FeNO à l’inclusion pouvait prédire la réduction du score et du volume de mucus en réponse au traitement par dupilumab.
Méthodes
Dans VESTIGE, un essai international de phase 4, randomisé, en double aveugle, contrôlé contre placebo, 109 adultes âgés de 21 à 70 ans atteints d’asthme modéré à sévère non contrôlé (score ACQ-5≥1,5, VEMS pré-bronchodilatateur≤80% de la valeur théorique, et≥1 exacerbation d’asthme au cours de l’année précédente) et présentant une inflammation de type 2 (éosinophiles sanguins≥300 cellules/μL et FeNO≥25 ppb) ont été randomisés selon un ratio 2 : 1 pour recevoir en traitement additionnel soit du dupilumab (300 mg en sous-cutané toutes les 2 semaines [dose de charge : 600 mg en sous-cutané]) soit un placebo de même volume toutes les 2 semaines pendant 24 semaines. Les variations du score et du volume de mucus chez les patients ayant une FeNO initiale < 50 ppb et≥50 ppb ont été analysées.
Résultats
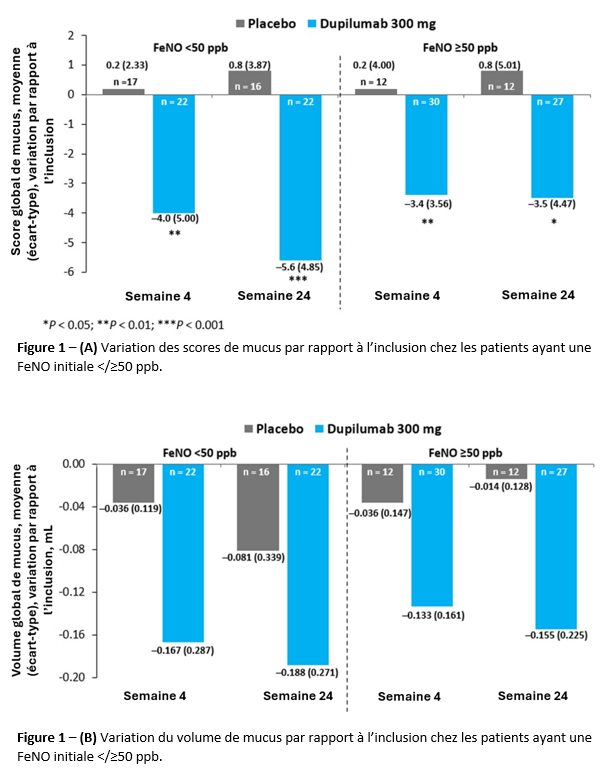
À la semaine 24, la diminution du score de mucus par rapport à l’inclusion était significativement plus importante avec le dupilumab qu’avec le placebo, et ce quel que soit la FeNO à l’inclusion (voir figure 1A). La diminution du volume de mucus entre l’inclusion et la semaine 24 était numériquement plus importante avec le dupilumab qu’avec le placebo, quel que soit la FeNO à l'inclusion (voir figure 1B).
Conclusion
Les patients atteints d’asthme modéré à sévère et présentant des biomarqueurs élevés d’inflammation de type 2 traités par dupilumab, étaient susceptibles de présenter une réduction du score et du volume de mucus à la semaine 24, indépendamment de la FeNO à l’inclusion (< 50 ppb ou≥50 ppb).
Bourdin A. * ; Pérez de Llano L.A. * ; Bhatt S.P. * ; Dunican E.M. * ; Lugogo N.L. * ; Castro M. * ; Papi A. * ; Comellas A.P. * ; Altincatal A. * ; Awad H. *
*Déclarent ne pas avoir de lien d'intérêt en rapport avec ce résumé.
