
Résumés CPLF 2026
Modifications de la structure/fonction des voies respiratoires sous benralizumab dans l’asthme sévère à éosinophiles, observées par Imagerie Fonctionnelle Respiratoire
Auteur correspondant : Ayinde D,
Introduction
L’inflammation éosinophilique contribue aux modifications des voies respiratoires dans l’asthme, notamment l’hypersécrétion de mucus et la réticulation/viscosité accrue du mucus, entrainant une augmentation du volume de mucus et du fardeau des symptômes. L’objectif de cette étude est d’évaluer les modifications structurelles et fonctionnelles des voies respiratoires chez des adultes atteints d’asthme sévère à éosinophiles suite à la déplétion éosinophilique induite par le benralizumab.
Méthodes
Cette étude de phase 4, multicentrique, mono-bras a inclus des adultes (18–70 ans) atteints d’asthme sévère à éosinophiles non contrôlé par une forte dose de corticostéroïdes inhalés et de β2-agoniste de longue durée d’action. Benralizumab 30 mg (SC) était administré toutes les 4 semaines (3 doses au total). Les scanners étaient analysés par Imagerie Fonctionnelle Respiratoire (IFR). Le critère d’évaluation principal, mesuré à la capacité pulmonaire totale, était la variation du volume total de mucus entre l’inclusion et la semaine 13. Les critères secondaires incluaient la variation des scores de bouchons muqueux et de la structure/fonction des voies respiratoires entre l’inclusion et la semaine 13.
Résultats
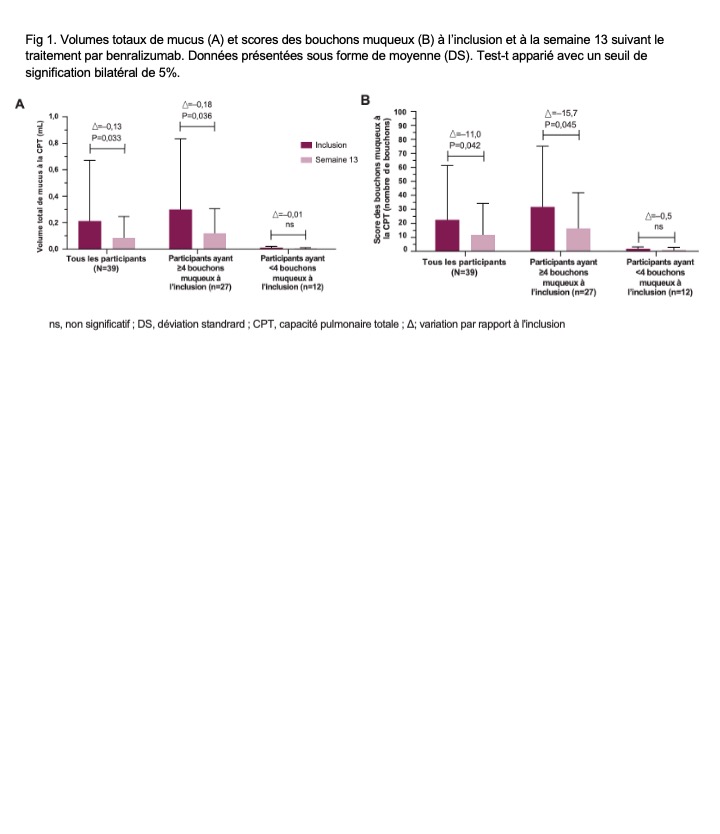
Le groupe d’analyse principal incluait 39 patients (moyenne [DS] 54,5 [11,4] ans). Le traitement par benralizumab était associé à une diminution du volume total de mucus chez la plupart des patients, avec une diminution plus marquée chez ceux ayant au moins 4 bouchons muqueux à l’inclusion (Fig 1A). De façon similaire, des réductions du score de bouchons muqueux ont été observées (Fig 1B). Aucune variation statistiquement significative par rapport à l’inclusion n’a été observée pour le piégeage gazeux, l’épaisseur de la paroi des voies respiratoires, le volume spécifique des voies respiratoires et le volume pulmonaire.
Conclusion
Une diminution des bouchons muqueux a été observée chez les patients asthmatiques sévères traités par benralizumab.
Bourdin A. a obtenu des financements et honoraires de consultations d'AstraZeneca-MedImmune, Boehringer-Ingelheim, Cephalon/Teva, GlaxoSmithKline, Novartis, Sanofi-Regeneron. Investigateur/co-investigateur pour des essais cliniques de AstraZeneca-MedImmune, Boehringer-Ingelheim, GlaxoSmithKline, Novartis, Regeneron- Sanofi, Chiesi, Actelion, Merck, Roche, Vertex, Galapagos. Membre du GINA ; Carstens D. employée d’AstraZeneca au moment de la réalisation de l’étude et de la rédaction du rapport, et pourraient détenir des actions ; DeBacker W. employé de FLUIDDA ; Rhodes K. employée d’AstraZeneca au moment de la réalisation de l’étude et de la rédaction du rapport, et pourraient détenir des actions ; Muchmore P. employé de FLUIDDA ; Lavon B.R. employé de FLUIDDA ; Chung S.Y.E. employé de FLUIDDA ; Fogel R. employé d’AstraZeneca au moment de la réalisation de l’étude et de la rédaction du rapport, et pourraient détenir des actions ; Trudo F. employé d’AstraZeneca au moment de la réalisation de l’étude et de la rédaction du rapport, et pourraient détenir des actions ; Panettieri Jr R. a reçu du soutien pour la recherche de, et a participé à des advisory boards pour AstraZeneca, Sanofi, Regeneron, Genentech et Novartis
