
Résumés CPLF 2026
Diagnostic et traitement systématique de la tuberculose résistante (TB-R) au centre hospitalier régional de Gaoua, Burkina Faso : analyse de cohorte hospitalière et revue de la littérature
Auteur correspondant : Maiga M.
Introduction
La tuberculose résistante à la rifampicine (TB-RR) constitue un défi majeur de santé publique au Burkina Faso. Les contraintes liées au diagnostic moléculaire limité et à l’accès restreint aux nouveaux antituberculeux compliquent la prise en charge des patients.
Méthodes
Nous avons analysé rétrospectivement les données hospitalières des patients suivis entre janvier 2021 et janvier 2025 pour tuberculose pulmonaire confirmée bactériologiquement avec résistance à la rifampicine détectée. Les données locales ont été comparées aux données récentes de la littérature.
Résultats
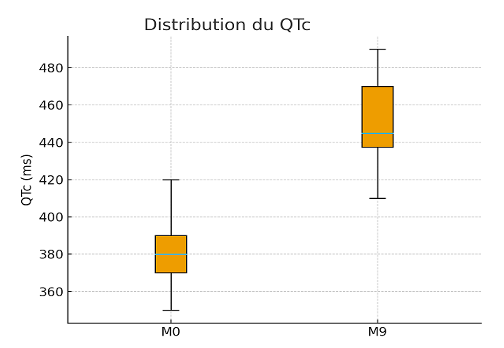
28 patients TB-RR ont été inclus. L’âge médian inférieur à 35 ans, prédominance masculine (86%). 64,28% des patients étaient naïfs d’un traitement antituberculeux (résistance primaire) traduisant une forte transmission communautaire. La recherche de résistance à l’isoniazide (INH) n’était pas systématique bien qu’il ait été utilisé dans le protocole national. L’absence de tests de sensibilité élargis aux fluoroquinolones (par mutation des gènes gyrA/gyrB), à l’isoniazide (par mutation des gènes katG, inhA) et aux nouveaux médicaments antituberculeux expose au risque d’inefficacité thérapeutique face à la circulation de mutants résistants, déjà rapportés pour la bédaquiline (Veziris, ERJ, 2017) et le prétomanide (Bateson, JAC, 2022). 96,3% des patients ont reçu le schéma court de 9 mois incluant la bédaquiline, sans test préalable de sensibilité aux fluoroquinolones. Une prolongation moyenne du QTc de +70 ms a été observée, avec 40% de QTc>450 ms mais aucun cas de QTc>500 ms. L’OMS recommande désormais des schémas oraux de 6 mois pour la TB-RR fluoroquinolone-sensible (Guglielmetti, NEJM, 2025). Leur mise en œuvre au Burkina Faso nécessitera un renforcement des capacités diagnostiques (génotypage, séquençage) et une surveillance accrue de la toxicité cardiaque. La mortalité dans la cohorte était de 10,7%.
Conclusion
La TB-RR à Gaoua illustre les défis diagnostiques et thérapeutiques rencontrés dans les pays à ressources limitées : une transmission communautaire élevée et un accès limité aux tests de résistance étendus. L’utilisation empirique des nouveaux antituberculeux expose aux risques de sélection de mutants et de toxicité. Le renforcement du diagnostic moléculaire et l’adoption des nouveaux protocoles OMS de 6 mois sont prioritaires pour améliorer le pronostic.
Références
[1] Veziris N, et al. Eur Respir J. 2017 ; 49(3):1601719
[2] Guglielmetti L, et al. N Engl J Med. 2025 ; 392 : 468-82,1
Maiga M. * ; Delma S-E. * ; Dabiré B. * ; Coulibaly A. * ; Combary A. * ; Boncoungou K. * ; Badoum G. * ; Ouédraogo M. *
*Déclarent ne pas avoir de lien d'intérêt en rapport avec ce résumé.
