
Résumés CPLF 2026
Étude rétrospective monocentrique de patients atteints d’une PID associé à cancer broncho-pulmonaire : facteurs de risque de mortalité et données moléculaires
Auteur correspondant : Pluvy J.
Introduction
Le cancer broncho-pulmonaire associé aux pneumopathies interstitielles diffuses (CBP-PID) est une entité avec un pronostic défavorable marqué par un risque compétitif entre exacerbation aiguë (EA) et un traitement oncologique sous-optimal [1]. Les séries occidentales sont limitées et les profils moléculaires peu décrits [2]. Nous rapportons une cohorte française afin d'identifier des déterminants indépendants de survie globale (SG) et préciser le paysage génomique.
Méthodes
Etude rétrospective monocentrique incluant tous les CBP-PID discutés en RCP d’oncologie thoracique à l’APHM entre 2010 et 2025. Les données démographiques, cliniques, fonctionnelles, radiologiques, histologiques et moléculaires ont été recueillies. La SG constituait le critère de jugement principal. Nous avons également analysé le moment du diagnostic de CBP par rapport à celui de l'ILD, l'intention du traitement (curatif vs non curatif) et la concordance entre les décisions de RCP et les traitements effectivement reçus. Les événements respiratoires aigus (ERA) ont été recensés ainsi que leur temporalité par rapport au traitement.
Résultats
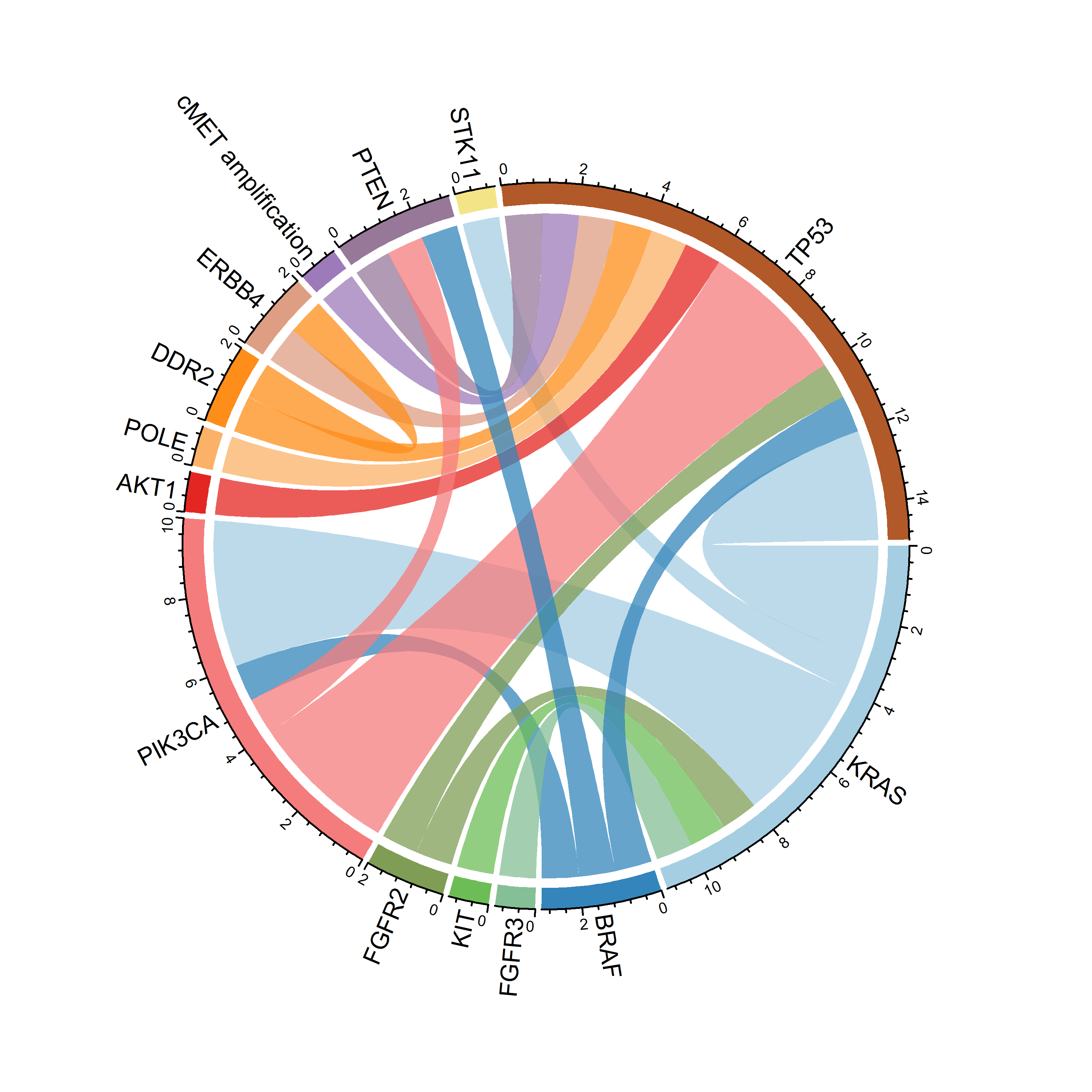
102 patients inclus : 83% d’hommes, âge médian 70 ans, 74% de fumeurs sevrés ou actifs. Le pattern radiologique dominant était la pneumopathie interstitielle commune (PIC) : 75% des cas avec une CVF et KCO médian respectivement de 76% et 64%. Le CBP survenait au cours du suivi d’une PID dans 55% des cas. Des ERA sont survenus chez 42% des patients avec 67% de mortalité le plus souvent en cours ou après un traitement. La SG médiane était de 17,7 mois (Taux de SG à 5 ans de 12,7%). En univarié la SG était réduite avec le tabagisme, la survenue d'un ERA, la diminution du KCO, un performans status (PS) altéré, l'absence de chirurgie, l'absence d’intention curative et le stade IV. En multivarié (modèle brut) les facteurs indépendants de survie était le KCO (%prédit) (HR 0,96 [0,95-0,98] p=0,001), un PS altéré (PS≥2 : (HR 3,78 [1,0-13,8] p=0,044), l'absence d'intention curative (HR 2,1 [1,1-3,9] p=0,02) et un tabagisme actif ou sevré (HR 3,08 [1,1-8,6] p=0,03). Un modèle avec imputation pour la CVF et le KCO par appariement prédictif des moyennes retrouvait le KCO, dont chaque augmentation de 1% réduisait le risque de décès de 3,6% ; IC95% [0,95–0,99] p< 0,001, le PS≥2 : (HR 8,88 [3,6-22,7] p< 0,001) et paradoxalement la concordance entre le traitement reçu et la proposition de RCP (HR 2,15 [1,14-4,0] p=0,018). Au plan moléculaire, nos résultats suggèrent un profil moléculaire distinct (figure), dominé par TP53, KRAS et les altérations de la voie PI3K avec des associations caractéristiques sans drivers ciblables identifiés.
Conclusion
Les CBP-PID sont de pronostic sombre avec des ERA fréquents et potentiellement sévères. Le KCO et le PS sont confirmés comme facteurs pronostiques robustes et indépendants de survie dans le CBP-PID quel que soit le stade ou l'intention du traitement. Le paysage moléculaire est dominé par TP53 KRAS et la voie PI3K qui sont souvent associés. L'intégration de paramètres comme le KCO et le PS permettent de guider la décision thérapeutique quel que soit le traitement proposé.
Références
[1] ERJ Open Res. 2022 Jun 20 ; 8(2):00115-2022
[2] Respir Res. 2017 Jun 15 ; 18(1):120
Goga A. * ; Soussi G. * ; Mogenet A. * ; Naud R. * ; Milesi J. * ; Coiffard B. * ; Habert P. * ; Fourdrain A. * ; Pollien E. * ; Gouton E. * ; Barboni M. * ; Tomasini P. * ; Greillier L. * ; Pluvy J. *
*Déclarent ne pas avoir de lien d'intérêt en rapport avec ce résumé.
