
Résumés CPLF 2026
Les patients atteints de polypose naso-sinusienne chronique (PNS) et d’asthme associé bénéficient de résultats précoces et durables du depemokimab dans les études ANCHOR-1/2
Auteur correspondant : Picaud C.
Introduction
Les symptômes de la PNS sont fréquemment induits par une inflammation de type 2, souvent associés à un asthme concomitant. Les patients atteints de PNS avec asthme associé présentent une forme plus sévère de la maladie et un taux de récidive plus élevé que ceux sans asthme. Le depemokimab est le premier anticorps monoclonal à ultra-longue durée d’action avec une forte affinité de liaison à l'interleukine-5, une puissance élevée et une demi-vie prolongée, permettant une inhibition soutenue de l’inflammation de type 2 et une administration 2 fois par an. L’efficacité du depemokimab vs placebo est décrite ici chez la sous-population de patients atteints de PNS et d’asthme associé issus de la population des essais de phase III ANCHOR-1/2.
Méthodes
Des adultes atteints de PNS insuffisamment contrôlée ont été randomisés (1 : 1) pour recevoir soit le depemokimab (100 mg en sous-cutané), soit un placebo, chacun avec un traitement d'entretien, toutes les 26 semaines pendant 52 semaines. Les co-critères principaux comprenaient la variation par rapport à l’inclusion du score endoscopique total de polypes nasaux (NPS, 0–8) à la semaine 52 et du score moyen d’obstruction nasale (échelle de réponse verbale [VRS], 0–3) sur les semaines 49–52. Les critères secondaires de perte d’odorat (VRS, 0–3) sur les semaines 49–52, de scores scanographiques Lund–Mackay (LMK, 0–24) à la semaine 52, et de délai jusqu’à la première chirurgie ou traitement modificateur de la maladie (DM) pour la PNS jusqu’à la semaine 52 (analyse post hoc) ont également été évalués.
Résultats
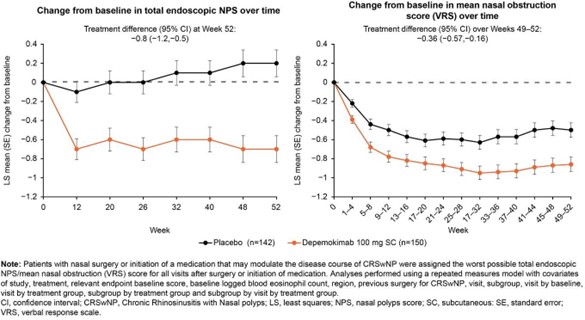
Un total de 528 patients (depemokimab, n=272 ; placebo, n=256) ont été inclus dans les études ANCHOR-1/2 ; 292 (depemokimab, n=150 ; placebo, n=142) présentaient un asthme associé. La variation moyenne selon les moindres carrés (LS) des co-critères principaux était plus importante pour le depemokimab comparé au placebo dès la première évaluation ; cette amélioration a été maintenue pendant 52 semaines (Figure). Les différences de traitement (depemokimab vs placebo) en variation LS moyenne par rapport à l’inclusion (IC 95%) étaient de –0,32 (–0,50, –0,14) pour la perte d’odorat (VRS) sur les semaines 49–52, et de –3,5 (–4,6, –2,3) pour le score LMK à la semaine 52. Une réduction de 75% du risque de recours à une chirurgie ou à un traitement DM pour PNS jusqu’à la semaine 52 a été observée pour le depemokimab par rapport au placebo (hazard ratio : 0,250 ; IC 95% : 0,114, 0,550).
Conclusion
Les effets du traitement ont été en faveur du depemokimab par rapport au placebo chez les patients atteints de PNS et d’asthme associé dans les études ANCHOR-1/2. Pour les co-critères principaux, les effets ont été observés précocement (dès la première évaluation) et ont été maintenus sur 52 semaines. Ces résultats soutiennent l’utilisation du depemokimab, administré deux fois par an, comme option thérapeutique pour les patients atteints de PNS et d’asthme associé.
Financement : GSK (217095/218079 ; NCT05274750/NCT05281523). Poster initialement présenté à l’EAACI, Glasgow, UK, 13-16 juin 2025
Mullol J. a reçu des subventions de recherche de GSK et Noucor/Uriach Group ; des honoraires de conseil de Sanofi Genzyme et Noucor/Uriach Group ; et a participé à des comités de conférenciers et/ou comités consultatifs pour Almirall, AstraZeneca, GSK, Menarini, MSD, Viatris, Regeneron Pharmaceuticals Inc.Sanofi Genzyme, UCB Pharma et Noucor/Uriach Group ; De Corso E. a reçu des honoraires pour des conférences et a participé à des comités d’experts de GSK, Novartis, Sanofi, Regeneron, Firma et AstraZeneca ; Cornet M. a reçu des honoraires de conférencier et a participé à des comités consultatifs pour Regeneron Pharmaceuticals Inc.Sanofi Genzyme, GSK, ALK et Stallergenes Greer ; Pfaar O. a reçu des subventions de GSK ; des subventions et/ou honoraires personnels et/ou un soutien pour ses déplacements de la part de AEDA, Alfried Krupp Krankenhaus, ALK-Abelló, Allergopharma, Almirall, Altamira Therapeutics, ASIT Biotech, AstraZeneca, Bencard Allergie GmbH/Allergy Therapeutics, Deutsche AllergieLiga e.V.Deutsche Forschungsgemeinschaft, Dustri-Verlag, ECM Expro ; Follows R. RF, DB, LW et PH sont employés de GSK et détiennent des parts financières dans GSK ; Brintziki D. RF, DB, LW et PH sont employés de GSK et détiennent des parts financières dans GSK ; Walrave L. RF, DB, LW et PH sont employés de GSK et détiennent des parts financières dans GSK ; Howarth P. RF, DB, LW et PH sont employés de GSK et détiennent des parts financières dans GSK ; Gevaert P. a participé à des comités consultatifs et a reçu des honoraires de conférencier de ALK-Abelló, Argenx, AstraZeneca, Genentech, GSK, Insmed, Lilly, Novartis, Regeneron, Roche, Sanofi Genzyme et Stallergenes Greer ; Malard O. a participé à des boards consultatifs pour SANOFI-Genzyme, ALK-Abello et GSK. Il communique et intervient pour Medtronic, GSK, Sanofi, Jonhson
