
Résumés CPLF 2026
Prévalence de la dyspnée d’effort et facteurs associés dans l’asthme sévère : données de la cohorte française RAMSES à l’inclusion
Auteur correspondant : Giovannelli J.
Introduction
La dyspnée d’effort contribue largement au fardeau des maladies respiratoires chroniques. Dans l’asthme sévère, il existe peu de données sur sa fréquence et ses déterminants. Les objectifs de l’étude étaient d’estimer la prévalence de la dyspnée d’effort dans l’asthme sévère, d’étudier ses facteurs associés, avec un focus sur le traitement par biothérapies.
Méthodes
La cohorte RAMSES est une cohorte multicentrique française de patients souffrant d’asthme sévère (selon la définition ATS-ERS 2014), inclus entre 2019 et 2024. Pour cette étude, le critère de jugement principal était le stade≥2 de l’échelle de dyspnée modifiée du Medical Research Council (mMRC) (dyspnée d’effort invalidante ou sévère), les critères secondaires les stades mMRC≥1 et≥3. Afin de limiter les biais de classement différentiels, nous avons exclu les centres présentant plus de 15% de valeurs manquantes sur cette variable. La prévalence globale a été calculée, ainsi que les prévalences stratifiées sur les principaux facteurs associés. Ceux-ci ont été évalués à l’aide d’un modèle de régression logistique, ajusté sur les principales covariables d’intérêt. Afin d’étudier la relation entre biothérapie et dyspnée d’effort, une analyse de médiation a été réalisée, sous l’hypothèse que l’efficacité potentielle des biothérapies reposait sur l’amélioration du contrôle de l’asthme. La relation entre biothérapie et dyspnée d’effort a été évaluée via deux modèles de régression logistique, avec et sans ajustement sur le score ACT, permettant le calcul du ratio de médiation (part de l’association expliquée par le score ACT).
Résultats
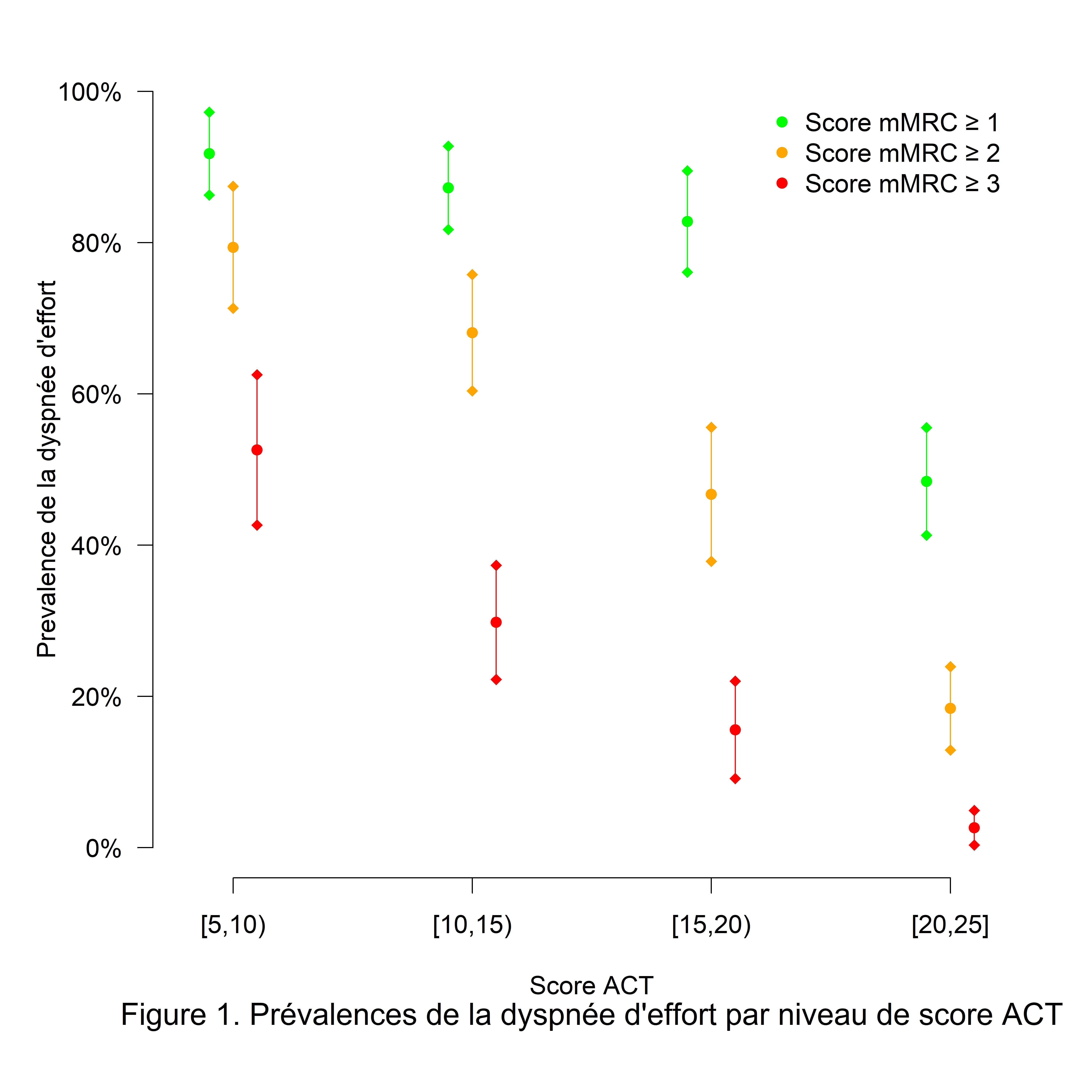
Nous avons inclus 569 des 2041 patients de la cohorte RAMSES. L’âge moyen était de 57,4 ans, la proportion de femmes de 63,1%, et le VEMS moyen de 73,4±22,8%. Un total de 360 (65,5%) patients étaient mal contrôlés (score de contrôle de l’asthme (ACT) < 20) et 307 (54,1%) étaient sous biothérapie depuis au moins 4 semaines. Les prévalences globales de la dyspnée d’effort définie par les stades mMRC≥1,≥2 et≥3 étaient respectivement de 73,8 [70,2 ; 77,4] %, 48,5 [44,4 ; 52,6] % et 21,6 [18,2 ; 25] %. Les prévalences stratifiées par niveau de score ACT sont représentées Figure 1.
Les principaux facteurs associés au stade mMRC≥2 étaient le score ACT (Odds ratio (OR)=0,8 [0,74 ; 0,86] pour une augmentation d’un point, p < 10-6), l’IMC (OR=2,9 [1,4 ; 6,3] surpoids vs poids normal, p=0,006 ; OR=4,7 [2,1 ; 10,9] obésité vs poids normal, p < 0,001) et la durée de l’asthme sévère (OR=1,7 [1,3 ; 2,4] par année supplémentaire, p < 0,001). Dans le modèle non ajusté sur le score ACT, la biothérapie était associée au stade mMRC≥2 (OR=0,46 [0,25 ; 0,84], p=0,011). Dans le modèle ajusté sur le score ACT, nous n’avons pas observé d’association entre biothérapie et stade mMRC≥2 (OR=0,75 [0,38 ; 1,49], p=0,41). Le ratio de médiation était de 63,4 [5 ; 254] %.
Conclusion
Dans l’échantillon d’étude, un patient sur deux présentait une dyspnée d'effort invalidante ou sévère. Le principal facteur de risque était le mauvais contrôle de l’asthme. L’IMC et la durée de la maladie étaient également associés. La prise d’une biothérapie était associée à une diminution de la dyspnée d’effort, les deux tiers de cette relation pouvant être expliqués par l’amélioration du contrôle de l’asthme.
Giovannelli J. déclare des honoraires personnels pour la participation à des boards de Boehringer-Ingelheim ; Perez T. déclare des honoraires personnels d'AstraZeneca, Chiesi, GSK, Sanofi pour des conseils consultatifs ou des présentations, une subvention de recherche d'Astra Zeneca ainsi qu'une aide au financement de congrès de Chiesi, Astra Zeneca, Sanofi, Viatrys et Vitalaire ; Garcia G. déclare des honoraires personnels d'ALK-Abello, d'AstraZeneca, de GSK, de Sanofi et une aide au financement de congrès de Sanofi et d'Oxyvie ; Devouassoux G. déclare des subventions d'AstraZeneca, GSK, Novartis, Sanofi, des honoraires personnels d'ALK-Abello, AstraZeneca, Celltrion, Chiesi, GSK, Sanofi et une aide au financement de congrès d'AstraZeneca, Chiesi, Novartis, Sanofi, GSK ; Fry S. déclare des honoraires personnels de GSK, Astrazeneca, Sanofi et une aide au financement de congrès de Sanofi ; Bourdin A. déclare des subventions d'Astra Zeneca, Boeringher Ingelheim, GSK ; des honoraires de consultation d'Astra Zeneca, GSK, Sanofi, Chiesi, Celltrion, Boeringher Ingelheim, Novartis ; des honoraires de Sanofi Regeneron, Astra Zeneca, GSK, Novartis, Boeringher Ingelheim ; une aide pour la participation à des réunions et/ou des déplacements d'Astra Zeneca, Sanofi ; une participation à un comité de surveillance de la sécurité des données ou à un comité consultatif d'AB science ; Chanez P. déclare des services de conseil pour GlaxoSmithKline, AstraZeneca, Celltrion, Chiesi, Sanofi et la SNCF ; a servi pour des comités de conseil pour Boehringer Ingelheim, GlaxoSmithKline, AstraZeneca, Chiesi, ALK, AB science, Argenx et Sanofi ; a reçu des honoraires pour des présentations de Boehringer Ingelheim, GlaxoSmithKline, AstraZeneca, Chiesi, ; a reçu des bourses de recherche de Roche, GlaxoSmithKline, AstraZeneca, ALK, et Novartis ; est président élu du conseil scientifique de la fondation du souffle(2020-2025) ; Bonniaud P. déclare avoir perçu des honoraires et/ou une prise en charge de frais de déplacement de la part des laboratoires AstraZeneca, GSK, Sanofi, Novartis, Chiesi, Boehringer-Ingelheim ; Boudjemaa A. déclare des subventions d'AstraZeneca, GSK, Sanofi, et une aide au financement de congrès d'AstraZeneca, Sanofi, GSK ; Saint-Raymond C. déclare une activité de consultante, de participation à des boards avec Novartis, GSK, AZ, Sanofi ; des EPU avec Novartis, AZ, GSK, Sanofi ; des congrès financés avec Chiesi, Boeringer Ingelheim, AGIRàdom, Resmed, Astra Zeneca, Sanofi, Jazz pharmaceutics ; Beurnier A. a reçu un paiement ou des honoraires pour des conférences, des présentations, la rédaction de manuscrits ou des événements éducatifs d'AstraZeneca et de Sanofi ; Bautin N. déclare des honoraires personnels d'AstraZeneca, GlaxoSmithKline, Sanofi et une aide au financement de congrès d'AstraZeneca, Chiesi, Menarini, Sanofi ; Taillé C. déclare avoir perçu des honoraires pour la participation à des boards, activité de conseil ou présentations de la part des laboratoires AstraZeneca, GSK, Sanofi, Chiesi, Stallergenes, Celltrion ; Chenivesse C. déclare des subventions d'AstraZeneca, GSK, Novartis, Santelys, des honoraires personnels d'ALK-Abello, AstraZeneca, Boehringer-Ingelheim, Celltrion, Chiesi, GSK, Sanofi et une aide au financement de congrès d'AstraZeneca, Boehringer-Ingelheim, Chiesi, Novartis, Sanofi ; RAMSES study group
