
Résumés CPLF 2026
Consensus institutionnel pour la prise en charge du cancer bronchique non à petites cellules de stade N2 ganglionnaire
Auteur correspondant : Eid H.
Introduction
Le cancer bronchique non à petites cellules (CBNPC) avec atteinte ganglionnaire médiastinale N2 est un facteur pronostique majeur dans les formes localisées. Sont classées N2 les atteintes ganglionnaires homolatérales et sous-carénaires. En l’absence d’approche universellement admise pour le diagnostic et le traitement, nous avons élaboré un consensus institutionnel pour la prise en charge du stade N2 au sein de l’Hôtel-Dieu de France (HDF).
Méthodes
Un groupe d’experts multidisciplinaire (pneumologie, oncologie, chirurgie thoracique, radiologie, médecine nucléaire, anatomopathologie, radiothérapie) a participé à un processus Delphi modifié après consentement éclairé.
Un comité de pilotage (3 relecteurs indépendants) a proposé 12 énoncés initiaux fondés sur les consensus internationaux, la littérature et l’expérience clinique.
Tour 1 : questionnaire ouvert, analyse thématique.
Tour 2 : cotation des énoncés générés + commentaires.
Tour 3 : cotation de l’accord sur échelle de Likert à 6 points.
Le consensus était défini par un accord≥80% (A+ ou A).
À l’issue de cette méthodologie, nous avons produit un organigramme décisionnel (flow-chart) opérationnel pour la pratique, soulignant l’importance d’une approche multidisciplinaire dans les cas N2.
Résultats
Dix-neuf médecins ont complété les trois tours. Un consensus complet a été obtenu pour 11/12 énoncés. Les principaux points d’accord étaient :
Bilan médiastinal préopératoire obligatoire chez les patients avec N2 résécable.
À considérer en cas de SUVmax élevé (≥3), de tumeurs proximales ou apicales et de taux élevés d’antigène carcino-embryonnaire.
Chirurgie sans traitement néoadjuvant possible en cas d’atteinte monostation non volumineuse et pour certaines tumeurs T3 invasives/T4 sélectionnées.
En cas d’atteinte multistation (N2), radiochimiothérapie comme traitement de base, suivie de Durvalumab chez les patients en bon état général.
En post-opératoire (pN2), la stratégie dépend de l’état des marges de résection.
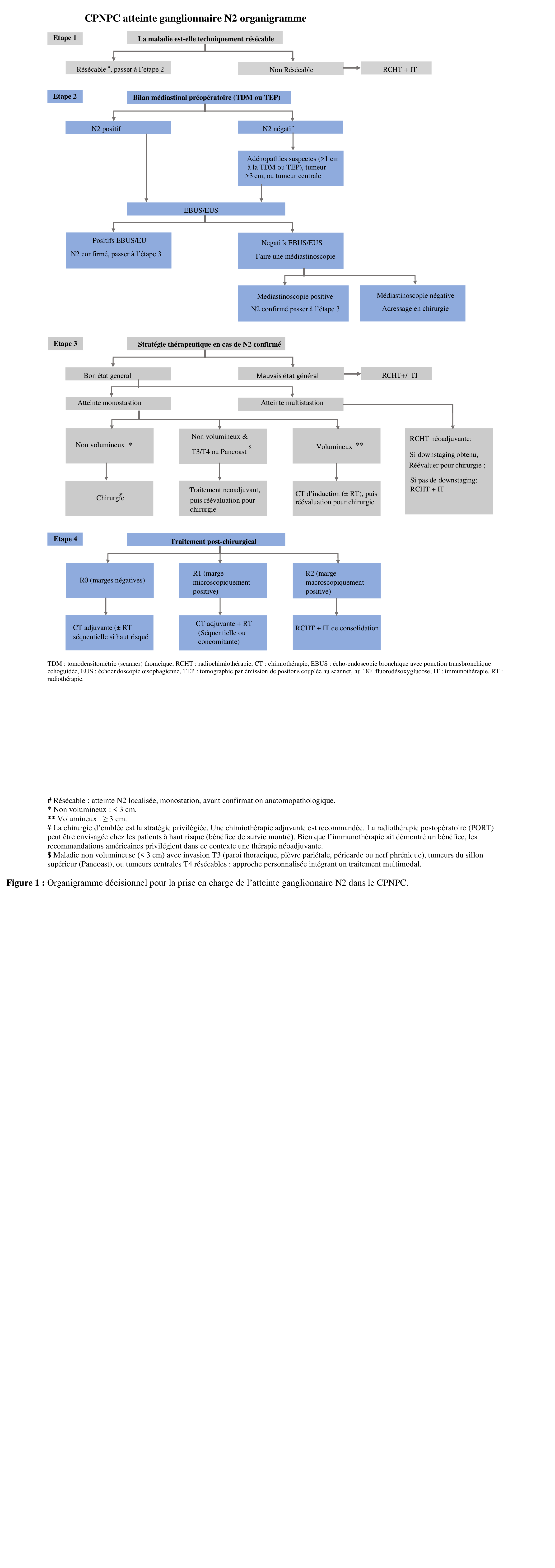
Cette approche a permis de formaliser un organigramme institutionnel dédié au stade N2 du CBNPC, servant de référentiel opérationnel en RCP (Figure 1)
Conclusion
Ce consensus institutionnel fournit un parcours diagnostico-thérapeutique standardisé pour le N2 du CBNPC, formalisé par un organigramme décisionnel. Il met ainsi en évidence que le recours à un Delphi modifié agrège de façon structurée et transparente l’expertise multidisciplinaire pour dégager un consensus pragmatique lorsque les preuves sont hétérogènes ou incomplètes, harmonisant ainsi la prise en charge des cas complexes.
Eid H. * ; Karam E. * ; El Kik A. * ; El Karak F. * ; Chamaa A. * ; Habr B. * ; Kourie H. * ; Azouri F. * ; Smayra V. * ; Aoun N. * ; Kattan J. * ; Chahine G. * ; Ghosn M. * ; Wakim J. * ; Nasserddine H. * ; Khayat G. * ; Nakad J. * ; Harmouche C. * ; Dabar G. * ; Tabet G. * ; Aoun Z. * ; Riachy M. *
*Déclarent ne pas avoir de lien d'intérêt en rapport avec ce résumé.
