
Résumés CPLF 2026
Efficacité et tolérance du nérandomilast chez des patients atteints d’une fibrose pulmonaire progressive associée à une maladie auto-immune : analyse de sous-groupes de l’essai FIBRONEER-ILD
Auteur correspondant : Lleu P.L.
Introduction
Le nérandomilast est un inhibiteur préférentiel de la phosphodiestérase 4B ayant des propriétés immunomodulatrices et antifibrotiques. L’essai de phase III FIBRONEER-ILD chez des patients atteints de fibrose pulmonaire progressive (FPP) a montré que le nérandomilast réduit de manière significative le déclin de la capacité vitale forcée (CVF) et avait un profil de sécurité acceptable. L'objectif est d'explorer l'efficacité et la tolérance du nérandomilast dans le sous-groupe de patients atteints de pneumopathies interstitielles diffuses associées (PID) à des maladies auto-immunes (AI) dans l’essai FIBRONEER-ILD chez les patients avec une FPP.
Méthodes
Les patients atteints de FPP (à l'exclusion des fibroses pulmonaires idiopathiques) ont été randomisées selon un rapport 1 : 1 : 1 pour recevoir 2 fois par jour du nérandomilast 9 mg ou 18 mg ou du placebo. La FPP a été définie à l'aide des mêmes critères que dans l'essai INBUILD [1]. Les patients prenant ou pas du nintédanib étaient éligibles à participer. L’utilisation des immunosuppresseurs/corticoïdes sont décrits dans [2]. Dans le sous-groupe des PID-AIs, ont été évalués la variation absolue de la CVF (mL) à la semaine 52 par rapport à la valeur initiale ; le délai jusqu’à la première exacerbation aiguë de la PID, l’hospitalisation pour cause respiratoire ou le décès jusqu’à la première fermeture de la base de données (DBL1) et les événements indésirables (EI) jusqu’à la DBL1. Ces analyses étaient prédéfinies.
Résultats
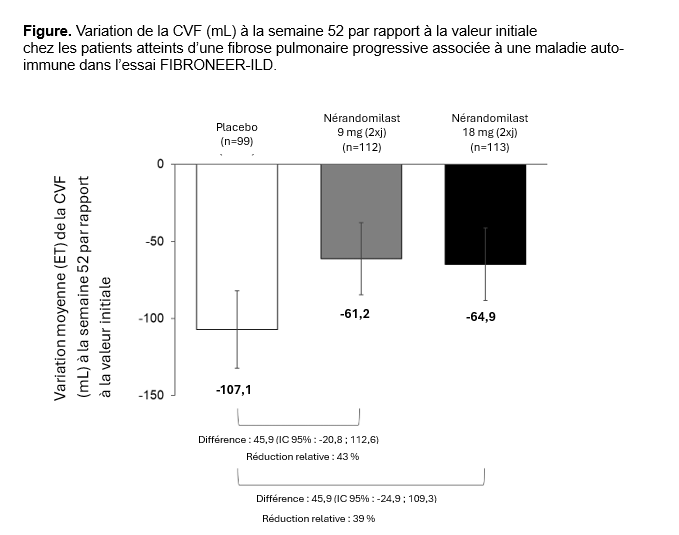
Parmi les 1176 patients traités, 325 présentaient une PID-AI (100 placebo, 112 nérandomilast 9 mg ou 113 nérandomilast 18 mg). À l’inclusion, parmi les patients atteints de PID-AI, 212 (65,2%) étaient des femmes, l’âge moyen (ET) était de 63,4 (11,2) ans, la CVF était de 71,5 (15,0) % de la valeur théorique, la capacité de diffusion du monoxyde de carbone était de 51,5 (16,8) %; 111 patients (34,2%) prenaient du nintédanib. Les maladies AIs les plus fréquentes étaient la polyarthrite rhumatoïde (118 patients [36,3%]), la sclérodermie systémique (75 [23,1%]) et les connectivites mixtes (47 [14,5%]). Les variations moyennes ajustées de la CVF (mL) à la semaine 52 sont décrites dans la Figure 1. L’exposition moyenne aux médicaments à l’étude jusqu’à la DBL1 était de 15 mois. Le hazard ratio vs placebo pour le délai jusqu’à la première exacerbation aiguë de la PID, l’hospitalisation pour cause respiratoire, ou le décès était de 0,71 (IC95%: 0,43 ; 1,20) pour le nérandomilast 9 mg et de 0,56 (IC95%: 0,33 ; 0,96) pour le nérandomilast 18 mg. Jusqu'à la DBL1 des EI graves ont été rapportés dans les groupes placebo, nérandomilast 9 mg et 18 mg, respectivement, chez 39,0%, 33,0% et 39,8% des patients et des EI ont conduit à l’arrêt du traitement chez 11,0%, 6,3% et 10,6% des patients. L’EI le plus fréquent était la diarrhée.
Conclusion
Dans l'essai FIBRONEER-ILD, l'efficacité du nérandomilast sur la réduction du déclin de la CVF chez les patients atteints de PID-AI était cohérente avec celle observée dans la population totale de l’étude. Le nérandomilast présentait un profil de tolérance acceptable, les EI graves et les arrêts de traitement n’étant pas plus fréquents chez les patients recevant du nérandomilast que du placebo.
Références
[1] NEJM 2019 ; 381 : 1718-27
[2] NEJM 2025 ; 392 : 2203-14
Cottin V. ; Hoffmann-Vold A.M. ; Assassi S. ; Kreuter M. ; Valenzuela C. ; Wijsenbeek M. ; Gu H. ; Ritter I. ; Stowasser S. ; Weimann G. ; Maher T.M.
