
Résumés CPLF 2026
Définition de la notion d’échec d’une biothérapie parmi les investigateurs de la cohorte RAMSES
Auteur correspondant : Valery S.
Introduction
Les arrêts de biothérapie pour « réponse insuffisante » sont fréquents dans l’asthme sévère. Cependant, il n’y a pas de consensus actuellement sur la définition de la réponse à une biothérapie, qui semble multimodale, mais une réduction de 50% des exacerbations et/ou de la corticothérapie est souvent utilisée comme un critère de réponse. L’objectif de cette étude est d’évaluer, en vie réelle, les critères d’échec retenus par les investigateurs de la cohorte française RAMSES.
Méthodes
Dans la cohorte d’asthme sévère RAMSES, les échecs de traitements sont définis par la décision d’arrêt d’une biothérapie avec la raison « Échec » cochée par l’investigateur. Les analyses ont été stratifiées selon la ligne de biothérapie (1ʳᵉ à 4ᵉ).
Résultats
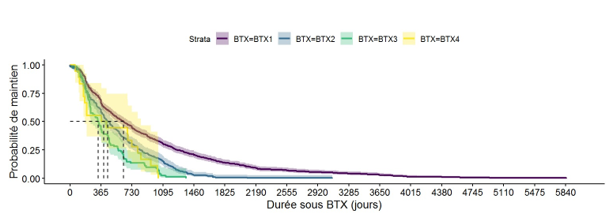
Parmi les 1764 patients analysés, 779 ont débuté une 1ere ligne de biothérapie après l’inclusion dans la cohorte, 592 une 2e et 257 une 3e ligne. Une décision d’arrêt a ensuite été prise pour respectivement 58%, 62% et 63%. L’échec en était la cause pour 195 (62,5%), 146 (69,2%) et 64 (70,3%) de ces patients. En 1ʳᵉ ligne, les échecs concernaient l’omalizumab (28 %), le mépolizumab ou le benralizumab (60 %) et le dupilumab (12 %) ; en 2ᵉ ligne, 15 patients sous omalizumab (10 %), 84 sous mepo/benralizumab (58 %), 44 sous dupilumab (30 %) et 3 sous tezepelumab (2 %) et en 3ᵉ ligne, 1 sous omalizumab (2 %), 36 sous mepo/benralizumab (56 %), 24 sous dupilumab (38 %) et 1 sous tezepelumab (2 %). La durée médiane avant décision d’arrêt était plus courte en 3ème ligne qu’en première ligne (379 (IQR 220-637) jours en 1ʳᵉ ligne contre 311 (IQR187-487) en 3ᵉ, p=0.047). Au moment de l’arrêt pour échec, le score ACT s’était amélioré par rapport à la valeur à l’initiation du traitement uniquement pour les 1e et 2e lignes (respectivement 12,4(SD 4,3) à 14,4(SD5,5), p<10-5 et 12,8(SD 4,9) à 14,3(SD5,7), p=0.005), sans atteindre des valeurs correspondant à un bon contrôle. Le nombre annuel moyen d’exacerbations restait stable (2,5(SD3,0) à 2,6(SD3,3) en 1ʳᵉ ligne (p=0,46) ; 2,9(SD3.8) à 3,0(SD3,5) en 2ᵉ (p=0.55), 2,7 (SD2,8) à 2,4(SD2,3) en 3ᵉ (p=0,67)). En revanche, le nombre annuel d’exacerbations sévères (avec recours aux urgences, hospitalisation ou séjour en réanimation) diminuait significativement (0,9(SD2,3) à 0,5(SD1,4) en 1ʳᵉ ligne (p=0.02) ; 0,9(SD2,1) à 0,6(SD1,5) en 2ᵉ (p=0,05) ; 1,0(SD2,2) à 0,6 (SD1,1) en 3ᵉ (p=0.03)). De plus, une réduction ≥50 % des exacerbations était observée chez 30,3% (59/195), 25,3% (37/146) et 23,4% (15/64) respectivement en 1ère, 2ème et 3ème ligne de traitement. Pour les exacerbations sévères, ces proportions étaient de 18,5 %, 19,2 % et 26,6 %. Aucune variation significative du VEMS n’était notée (2,08L(0,84) à 2,18L(0,79) en 1ère ligne (p=0,24), de 2,05L(0 ,93) à 2,19L(0,82) en 2e (p=0,08) et de 2,07L(0,92) à 1,95L(0,84) en 3ème ligne (p = 0,09)).
Conclusion
Les décisions d’arrêts de biothérapie sont fréquentes dans la cohorte RAMSES et l’échec du traitement en est la raison principale. La stratégie d’utilisation des biothérapies est hétérogène, avec notamment une définition de l’échec du traitement qui semble variable selon les praticiens.
Valery S. ; Simon-Tillaux N. ; Devouassoux G. ; Chenivesse C. ; Bonniaud P. ; Chanez P. * ; Boudjemaa A. ; Estellat C. ; Taillé C. ; et le RAMSES Study Group
*Déclare ne pas avoir de lien d'intérêt en rapport avec ce résumé.
