
Résumés CPLF 2026
Depemokimab, administré deux fois par an, est bien toléré dans les études de phase III SWIFT et ANCHOR
Auteur correspondant : Picaud C.
Introduction
Depemokimab est le premier médicament biologique à ultra-longue durée d’action doté d'une affinité de liaison à l'IL-5 améliorée, d'une puissance élevée et d'une demi-vie prolongée, permettant une administration 2 fois par an. Les études SWIFT-1/2 et ANCHOR-1/2 ont démontré l'efficacité du depemokimab chez des patients atteints d'asthme éosinophile de type 2 et chez des patients atteints d'une polypose naso-sinusienne insuffisamment contrôlée (PNS), respectivement ; dans chacune de ces études, la proportion de patients présentant un événement indésirable (EI) était comparable dans tous les groupes de traitement. L'objectif de cette étude est d'évaluer la tolérance du depemokimab dans les données groupées SWIFT/ANCHOR.
Méthodes
Des patients âgés de≥12 ans (SWIFT)/≥18 (ANCHOR) randomisés 2 : 1/1 : 1, respectivement, ont reçu 100 mg de depemokimab par voie sous-cutanée ou un placebo, en addition du traitement standard, toutes les 26 semaines pendant 52 semaines.
Résultats
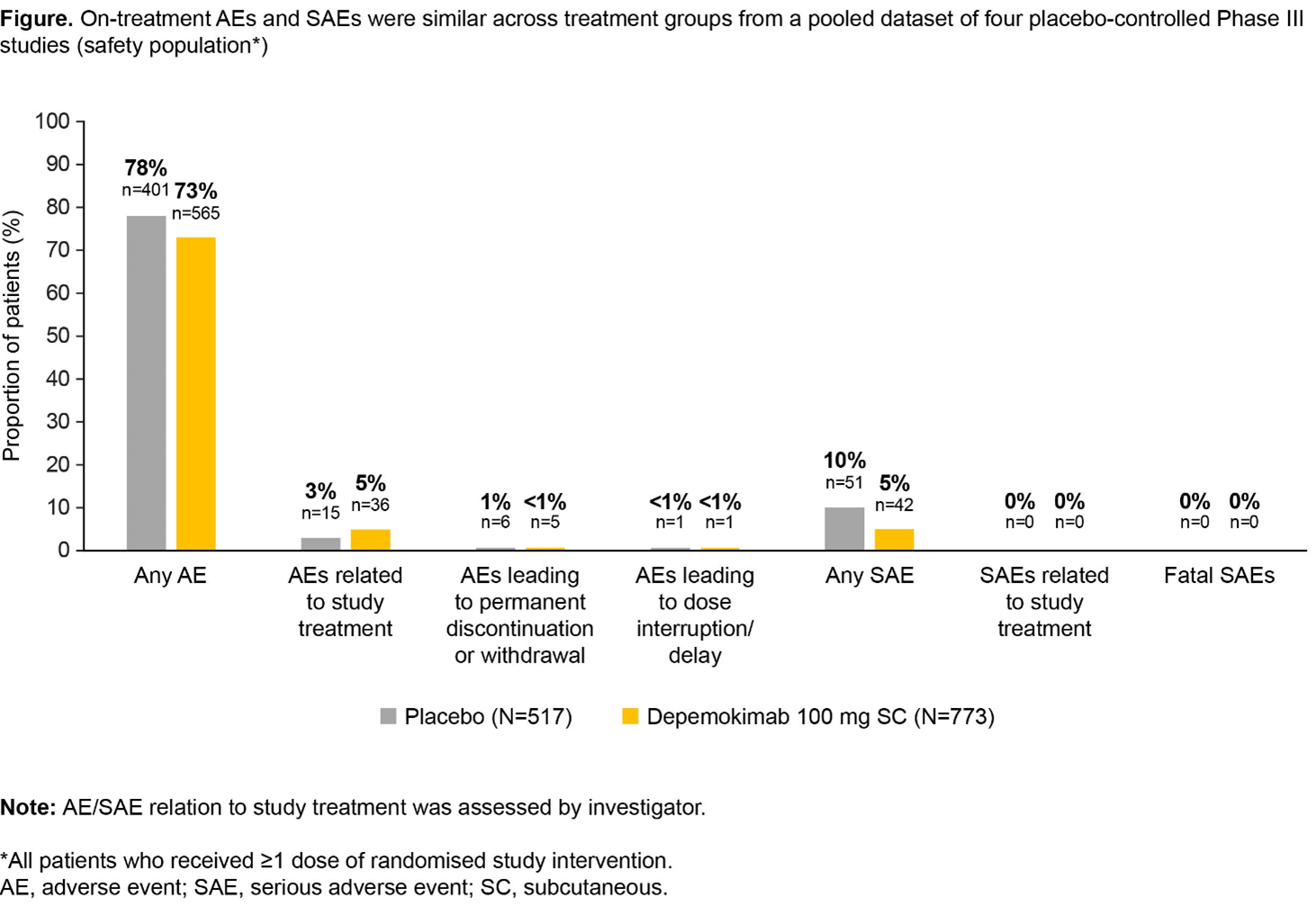
Sur 773 patients traités par depemokimab et 517 patients sous placebo dans la population regroupée SWIFT/ANCHOR, 713 (92%) et 461 (89%) ont terminé le traitement/L'étude, respectivement. L'exposition moyenne était de 11,7 mois (écart-type 1,5) dans les deux groupes de traitement. La proportion de patients présentant des EI en cours de traitement et des EI graves (EIG) était similaire dans les deux groupes de traitement, sans EIG mortels ou liés au traitement (Figure).
Conclusion
Depemokimab, administré deux fois par an, est bien toléré chez les patients asthmatiques ou atteints de PNS, confirmant l'innocuité du premier traitement biologique à ultra-longue durée d’action dans ces populations.
Financement : GSK 206713/213744/217095/218079 ; NCT04719832/NCT04718103/NCT05281523/NCT05274750. Poster initialement présenté à l’ERS, Amsterdam, Pays-bas, 27 septembre-1er octobre 2025
Cornet M. a reçu des honoraires de conférencier et a participé aux réunions du conseil consultatif de Regeneron Pharmaceuticals Inc.Sanofi Genzyme, GSK, ALK, Chiesi et Stallergenes Greer ; Bourdin A. a reçu des subventions de GSK, de Boehringer Ingelheim et d'AstraZeneca, a participé à des projets de recherche clinique (en tant que chercheur) avec GSK, AstraZeneca, Boehringer Ingelheim, Chiesi, Novartis, Acceleron, Gossamer, Pfizer, MSD et Sanofi, et a reçu des honoraires personnels pour des conseils consultatifs et d'autres réunions de GSK, AstraZeneca, Amgen, Regeneron-Sanofi, Novartis, Celltrion et Chiesi ; Bird N. NB, DE, NK, RF, DM, AV, LW et PH sont des employés de GSK et détiennent des actions financières dans GSK ; Edwards D. NB, DE, NK, RF, DM, AV, LW et PH sont des employés de GSK et détiennent des actions financières dans GSK ; Karkoszka N. NB, DE, NK, RF, DM, AV, LW et PH sont des employés de GSK et détiennent des actions financières dans GSK ; Follows R. NB, DE, NK, RF, DM, AV, LW et PH sont des employés de GSK et détiennent des actions financières dans GSK ; Muccino D. NB, DE, NK, RF, DM, AV, LW et PH sont des employés de GSK et détiennent des actions financières dans GSK ; Vichiendilokkul A. NB, DE, NK, RF, DM, AV, LW et PH sont des employés de GSK et détiennent des actions financières dans GSK ; Walrave L. NB, DE, NK, RF, DM, AV, LW et PH sont des employés de GSK et détiennent des actions financières dans GSK ; Howarth P. NB, DE, NK, RF, DM, AV, LW et PH sont des employés de GSK et détiennent des actions financières dans GSK ; Jackson DanJ a été consultant et a reçu des subventions de Regeneron, Sanofi et GSK, a consulté et DSMB pour AstraZeneca, a été consultant pour Areteia, Avillion et Genentech (2022), et a reçu une subvention d'OM Pharma et de DSMB pour Upstream Bio ; Lahmar Z. *
*Déclare ne pas avoir de lien d'intérêt en rapport avec ce résumé.
