
Résumés CPLF 2026
Données en vie réelle : résultats cliniques de l’asthme, furoate de fluticasone/vilantérol (FF/VI) comparé au dipropionate de beclometasone /formoterol (BDP/FOR)
Auteur correspondant : Gutierrez-Mateyron E.
Introduction
La comparaison en vraie vie du FF/VI vs BDP/FOR chez les patients naïfs de corticostéroïdes inhalés/β2-agonistes à longue durée d’action est limitée. Cette étude avait pour objectif de comparer l’administration de FF/VI vs BPD/FOR en vraie vie chez des patients atteints d’asthme en Angleterre.
Méthodes
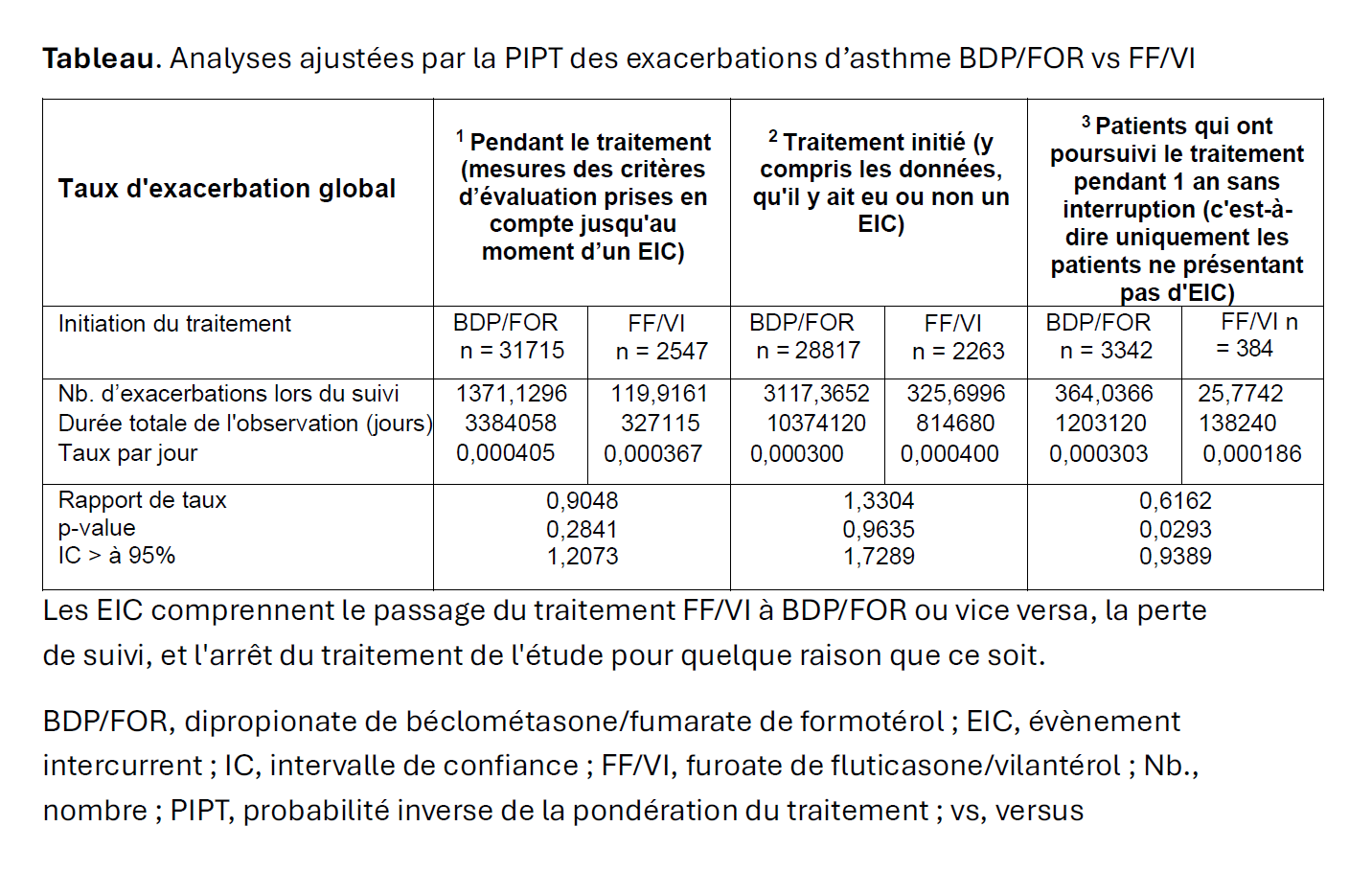
Etude rétrospective portant sur des adultes (âgés de 18 ans ou plus) atteints d’asthme débutant un traitement par FF/VI ou par BDP/FOR (traitement régulier ou traitement d’entretien et de secours) entre le 1er décembre 2015 et le 28 février 2019, identifiés à partir de l’ensemble de données issues de la Clinical Practice Research Datalink-Hospital Episode Statistics en Angleterre. La date index était celle de la première prescription de l’un ou l’autre des médicaments ; le suivi était inférieur à 12 mois. Les patients éligibles avaient reçu au moins une prescription de β2-agonistes à courte durée d’action au cours des six mois précédant la date index et étaient suivis de manière continue auprès d’un médecin généraliste depuis au moins 12 mois avant la date index. Les critères d’exclusions comprenaient la BPCO. Critère de jugement principal : toutes les exacerbations d’asthme. Un ajustement par pondération de la probabilité inverse du traitement a été appliquée pour les facteurs de confusion inégaux à l’inclusion ; les populations analysées1-3sont décrites dans le Tableau.
Résultats
Les patients ayant initié un traitement par FF/VI présentaient un taux d’exacerbation numériquement similaire à celui des patients sous BDP/FOR dans la population ayant commencé le traitement2, inférieur dans la population lorsque le résultat était mesuré jusqu’à un évènement1, et significativement inférieur chez les patients poursuivant le traitement pendant 1 an sans interruption3 (FF/VI [n=384] vs BPD/FOR [n=3342] ; Tableau).
Conclusion
Après un traitement ininterrompu pendant 1 an, le FF/VI a été associé à moins d’exacerbations par rapport au BDP/FOR.
Bourdin A. a reçu des subventions, des honoraires personnels, un soutien non financier et d'autres soutiens d'Actelion, d'AstraZeneca, de Boehringer Ingelheim et de GSK ; des honoraires personnels, un soutien non financier et d'autres soutiens de Chiesi, Novartis et Regeneron ; les honoraires personnels et le soutien non financier de Teva ; les honoraires personnels de Gilead ; soutien non financier et autres soutiens de Roche ; et d'autres formes de soutien de Nuvaira ; Woodcock A. a donné des conférences pour Orion et a été consultant pour GSK et Orion ; Blakey J. fait état de subventions ou de contrats d'AstraZeneca, de GSK et de Novartis ; les honoraires de consultation de Boehringer Ingelheim, Chiesi et GSK ; paiement ou honoraires d'AstraZeneca, de Chiesi et de GSK ; l'aide d'AstraZeneca, de Boehringer Ingelheim et de GSK pour la participation à des réunions et/ou des déplacements ; l'obtention d'un soutien à la rédaction médicale de GSK et de Teva ; le paiement à leur établissement pour le travail consultatif d'Asthma Australia ; et le travail de conseil non rémunéré d'Asthma WA ; Canonica GW. déclare avoir reçu des subventions de recherche en plus d'être chargé de cours ou d'avoir reçu des honoraires au conseil consultatif de : A.Menarini Diagnostics, Allergy Therapeutics, AstraZeneca, Chiesi, Faes, Firma, Genentech, Guidotti– Malesci, GSK, Hal Allergy, Innovacaremd, Novartis, OmPharma, RedMaple, Sanofi– Aventis, Sanofi– Genzyme, Stallergenes– Greer et Uriach Pharma ; Domingo C. déclare avoir reçu une aide financière pour l'aide au voyage et les bureaux des conférenciers de la part d'ALK-Abello, Allergy Therapeutics, AstraZeneca, Chiesi, GSK, Hall Allergy, Inmunotek, A.Menarini Diagnostics, MSD, Novartis, Roxall, Sanofi et Stallergenes ; Ford A. est un employé d'Adelphi Real World, qui a reçu un financement de GSK pour cette étude ; Hulme R. est une employée d'Adelphi Real World, qui a reçu un financement de GSK pour cette étude ; Tritton T. est un employé d'Adelphi Real World, qui a reçu un financement de GSK pour cette étude ; Vinall E. est une employée d'Adelphi Real World, qui a reçu un financement de GSK pour cette étude ; Palomares I. est une employée de GSK et détient des participations financières dans GSK ; Sadhu S. est une employée de GSK ; Biswas A. est un employé de GSK et détient des participations financières dans GSK ; Verrma M. est un employé de GSK et détient des participations financières dans GSK
