
Résumés CPLF 2026
Mepolizumab est efficace chez les patients atteints de BPCO, quel que soit le phénotype clinique : analyse post hoc de l'essai de phase III MATINEE
Auteur correspondant : Saidi H.
Introduction
La bronchopneumopathie chronique obstructive (BPCO) est st une maladie hétérogène avec différents sous-types : bronchite chronique (BC ; inflammation des voies respiratoires), emphysème ou une combinaison des deux. L’essai MATINEE a évalué l’efficacité du mepolizumab, un anticorps monoclonal ciblant l’interleukine-5, chez des patients atteints de BPCO, indépendamment du sous-type rapporté par l’investigateur.
Méthodes
MATINEE (NCT04133909), essai de phase III randomisé en groupes parallèles, a inclus des patients atteints de BPCO avec antécédents d’exacerbations et taux d’éosinophiles sanguins≥300 cellules/µL lors du dépistage. Les participants ont été randomisés 1 : 1 pour recevoir soit du mepolizumab toutes les 4 semaines pendant 52 à 104 semaines, soit un placebo, en complément d’une triple thérapie inhalée optimale (double bronchodilatateurs à action prolongée + corticostéroïde inhalé [propionate de fluticasone≥500 μg/jour ou équivalent]). Les investigateurs ont rapporté le sous-type clinique via un formulaire électronique. Les analyses post hoc incluaient le taux d’exacerbations modérées/graves (« modérées » : traitées par corticostéroïdes systémiques et/ou antibiotiques ; « graves » : hospitalisation≥24 heures ou décès), les exacerbations nécessitant une visite aux urgences et/ou une hospitalisation, ainsi que les changements au score SGRQ (questionnaire respiratoire de St George) à la semaine 52 (« réponse » : amélioration≥4 points), stratifiés par sous-type.
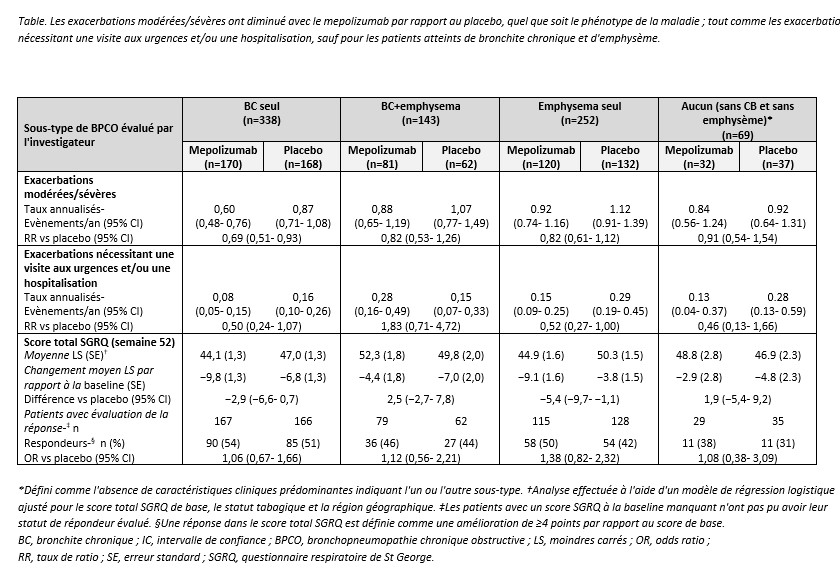
Résultats
804 patients ont été randomisés (403 mépolizumab/401 placebo). Parmi eux, 42% (338) présentaient uniquement BC, 18% (143) BC+emphysème, 31% (252) emphysème seul et 9% (69) aucun des deux. Les taux d’exacerbations modérées/graves étaient réduits avec le mepolizumab, la plus forte réduction relative (31%) étant observée dans le sous-groupe BC (rate ratio [IC95%] : 0,69 [0,51-0,93]). Les exacerbations nécessitant une visite ED/hospitalisation ont diminué de 50% (0,50 [0,24-1,07]), 48% (0,52 [0,27-1,00]) et 54% (0,46 [0,13-1,66]) dans les sous-groupes BC, emphysème et aucun des deux, respectivement (Table). L’effet inverse a été observé dans le sous-groupe BC+emphysème (1,83 [0,71-4,72]). Le score SGRQ s’est amélioré numériquement dans tous les sous-groupes, avec des bénéfices du mepolizumab dans les sous-groupes BC et emphysème. Les réponses au SGRQ étaient également meilleures dans ces sous-groupes, particulièrement dans celui emphysème.
Conclusion
En conclusion, le mepolizumab, en complément de la triple thérapie inhalée, a réduit les exacerbations chez les patients atteints de BPCO, avec des effets prononcés pour les visites ED/hospitalisations dans les sous-groupes BC et emphysème. Ces données pourraient orienter l’identification des populations à forte réponse à la thérapie biologique dans la BPCO.
Bourdin A. ; Pavord I-D. ; Christenson S-A. ; Min J. ; Kolterer S. ; Mayer B. ; Singh D.
