
Résumés CPLF 2026
Variation régionale de la réponse au depemokimab par rapport au placebo chez les patients asthmatiques avec inflammation de type 2 : analyse en sous-groupes des études de phase III SWIFT-1/2
Auteur correspondant : Picaud C.
Introduction
Dans plusieurs essais contrôlés portant sur des traitements de l'asthme, des variations régionales de l'ampleur de la réponse au placebo ont été observées, pouvant refléter des différences dans les structures du système de santé pour les patients asthmatiques. Le depemokimab est le premier médicament biologique à ultra longue durée d’action avec une affinité de liaison à l'interleukine-5 améliorée, une puissance élevée et une demi-vie prolongée, permettant une administration deux fois par an chez les patients asthmatiques. Dans les études de phase III SWIFT-1/2, le depemokimab a significativement réduit les exacerbations avec une inhibition soutenue de l'inflammation de type 2 observée chez les patients atteints d'asthme éosinophilique de type 2 [1]. Une variation régionale de l'efficacité a été observée dans les analyses préliminaires ; à ce titre, des analyses post hoc ont été menées pour explorer l'impact de la variation régionale sur les résultats de SWIFT-1/2.
Méthodes
Des analyses pré-spécifiées et post hoc des études SWIFT-1/2 [1] ont été menées pour étudier les taux d'exacerbation annualisés et l'évolution entre l’inclusion et la semaine 52 du score SGRQ (St George's Respiratory Questionnaire) par région.
Résultats
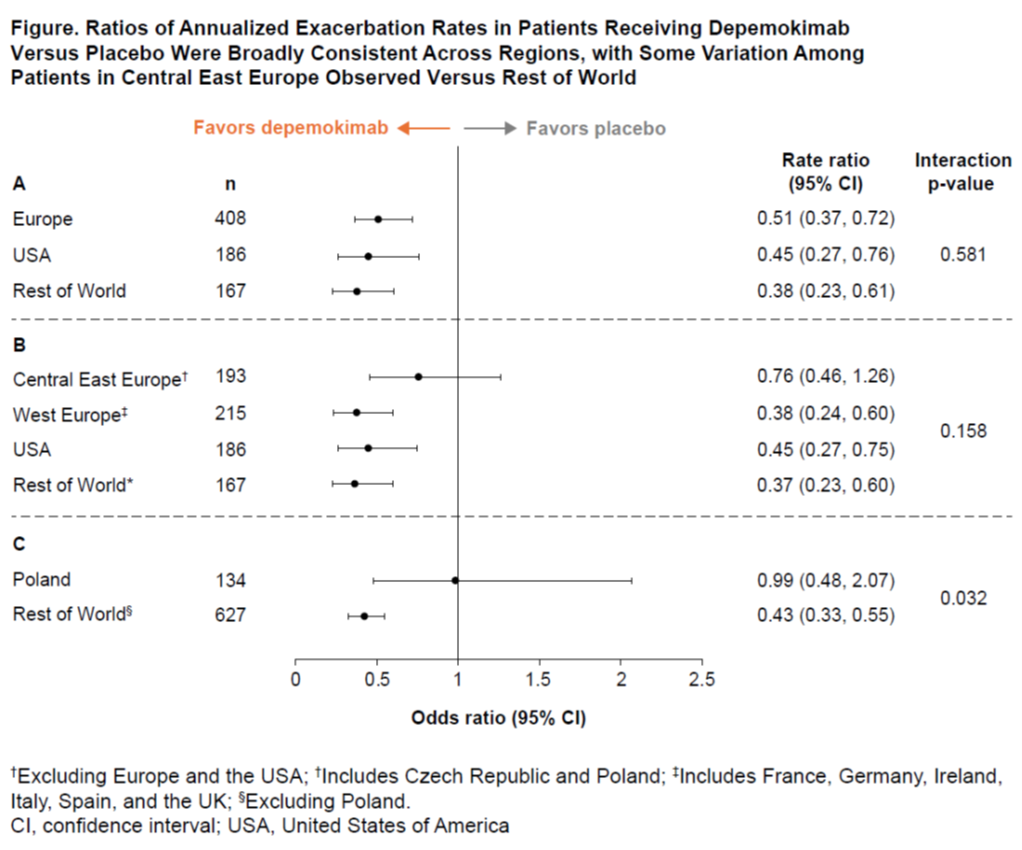
Des patients (N=762) ont été recrutés dans 16 pays pour l'étude SWIFT-1/2, avec une moyenne (écart-type) de 2,4 (1,46) exacerbations au cours de l'année précédente. Dans une analyse de sous-groupe préspécifiée, la réduction du taux d'exacerbation chez les patients traités par le depemokimab par rapport au placebo était globalement cohérente chez les patients recrutés en Europe, aux États-Unis et dans le reste du monde (Figure A). Dans les analyses post hoc, des réductions du taux d'exacerbation numériquement plus faibles (intervalle de confiance à 95%) ont été observées chez les patients d'Europe de l’Est par rapport à l'Europe de l'Ouest, aux États-Unis et dans le reste du monde (Figure B), et de la Pologne par rapport au reste du monde (Figure C), en raison de faibles taux d'exacerbation dans le groupe placebo en Europe de l’Est (depemokimab : 0,50 [0,37, 0,69] vs placebo : 0,66 [0,44, 0,99]) et en Pologne (depemokimab : 0,33 [0,22, 0,51] vs placebo : 0,34 [0,18, 0,62]). Dans le reste du monde (en excluant la Pologne), les taux d'exacerbation étaient de 0,55 (0,47, 0,66) et de 1,30 (1,07, 1,58) pour le depemokimab et le placebo, respectivement. Des profils de réponse placebo similaires ont été observés pour le changement par rapport à l’inclusion sur le SGRQ à la semaine 52.
Conclusion
L'efficacité du depemokimab administré deux fois par an dans les essais SWIFT-1/2 était globalement cohérente dans toutes les régions. Cependant, une réduction différente des exacerbations a été observée chez les patients d'Europe de l’Est, où il y avait une réponse substantielle au placebo, par rapport à d'autres régions. Cette observation pourrait refléter des variations dans la pratique clinique et l'adhésion aux thérapies de fond avant le début de l'essai. Les différences régionales dans la réponse au traitement pourraient également être dues à l'accès aux traitements biologiques (en raison des règles d'arrêt ou des critères de remboursement), entraînant des différences dans les populations de patients participant aux essais cliniques au fil du temps.
Financement : GSK (206713/213744 ; NCT04719832/NCT4718103). Poster initialement présenté à l’ATS, San Francisco, Etats-Unis, 18-21 mai 2025
Références
[1] Jackson DJ et al. NEJM 2024 ; 10,1056/NEJMoa2406673.
Jackson DavJ a reçu des honoraires de conseil et/ou de prise de parole de la part de GSK, AstraZeneca et Sanofi Regeneron ; Lugogo NL. a reçu des honoraires de conseil de la part d’Amgen, AstraZeneca, Avillion, Genentech, GSK, Niox, Novartis, Regeneron, Sanofi et Teva ; des honoraires pour des présentations hors du cadre des speakers bureaux de GSK, Teva et AstraZeneca ; ainsi qu’un soutien pour ses déplacements de la part d’AstraZeneca, Sanofi, Teva, Regeneron et GSK. Son institution a reçu un soutien à la recherche de la part d’Amgen, AstraZeneca, Avillion, Bellus, Evidera, Gossamer Bio, Genentech, GSK, Janssen, Niox, Regeneron, Sanofi, Novartis et Teva. Elle est membre honoraire du corps enseignant de l’Observational and Pragmatic Research Institute (OPRI), mais ne perçoit aucune rémunération pour ce rôle ; Kuna P. a reçu des honoraires pour des prises de parole de la part d’AstraZeneca, GSK, Chiesi, Sanofi, Novartis et Boehringer Ingelheim ; Jacques L. LJ, NB, TF-H et PH sont employés de GSK et détiennent des participations financières dans l’entreprise ; Bird N. LJ, NB, TF-H et PH sont employés de GSK et détiennent des participations financières dans l’entreprise ; Finney-Hayward T. LJ, NB, TF-H et PH sont employés de GSK et détiennent des participations financières dans l’entreprise ; Howarth P. LJ, NB, TF-H et PH sont employés de GSK et détiennent des participations financières dans l’entreprise ; Jackson DanJ a été consultant et a reçu une subvention de Regeneron, Sanofi et GSK, a été consultant et membre d’un comité de surveillance des données (DSMB) pour AstraZeneca, a été consultant pour Areteia, Avillion et Genentech (en 2022), a reçu une subvention de OM Pharma, et a été membre d’un DSMB pour Upstream Bio ; Ahmed E. a reçu des honoraires de conseil et/ou de prise de parole de la part de Astrazeneca et Sanofi
