
Résumés CPLF 2026
Efficacité du brensocatib chez les patients atteints de dilatation des bronches : analyse en sous-groupes de l’étude ASPEN en fonction du taux d’éosinophiles sanguins
Auteur correspondant : Burgel P-R.
Introduction
L’inflammation neutrophilique joue un rôle clé dans la physiopathologie des dilatations des bronches. Les protéases à sérine des neutrophiles (PSN) sont associées à la progression de la maladie et à une moins bonne évolution clinique. Le brensocatib, un inhibiteur oral, compétitif et réversible de la dipeptidyl peptidase 1, empêche l’activation des PSN. Dans l’étude de phase 3 ASPEN (NCT04594369), l’administration quotidienne de brensocatib, 10mg et 25mg par voie orale, a réduit de manière significative le taux annualisé d’exacerbations pulmonaires (ExP) évaluées sur 52 semaines par rapport au placebo ; la dose de 25mg a également réduit de manière significative le déclin de la fonction pulmonaire et amélioré de manière nominale les symptômes rapportés par les patients. L’éosinophilie est présente chez ~20% des patients atteints de bronchectasie. Nous présentons ici les résultats d’une analyse en sous-groupe de patients de l’étude ASPEN en fonction du nombre d’éosinophiles à l’inclusion.
Méthodes
Les patients atteints de dilatations des bronches avec des antécédents d’ExP au cours des 12 mois précédant l’inclusion (adultes≥2/an, adolescents≥1/an) ont quotidiennement reçu du brensocatib (10mg ou 25mg) ou un placebo pendant 52 semaines. Les patients ont été séparés en deux sous-groupes en fonction du nombre d’éosinophiles (EOS) dans le sang lors de l’inclusion : EOS élevé (≥300/μl) ou EOS faible (< 300/μl). Les critères d’évaluation étaient le taux annualisé d’ExP, le délai jusqu’à la première ExP, la proportion de patients sans ExP, le taux d’ExP sévères, la variation du volume expiratoire maximal par seconde (VEMS) après bronchodilatateur et de la capacité vitale forcée (CVF), ainsi que la variation du score de qualité de vie de la bronchectasie (QOL-B RSS).
Résultats
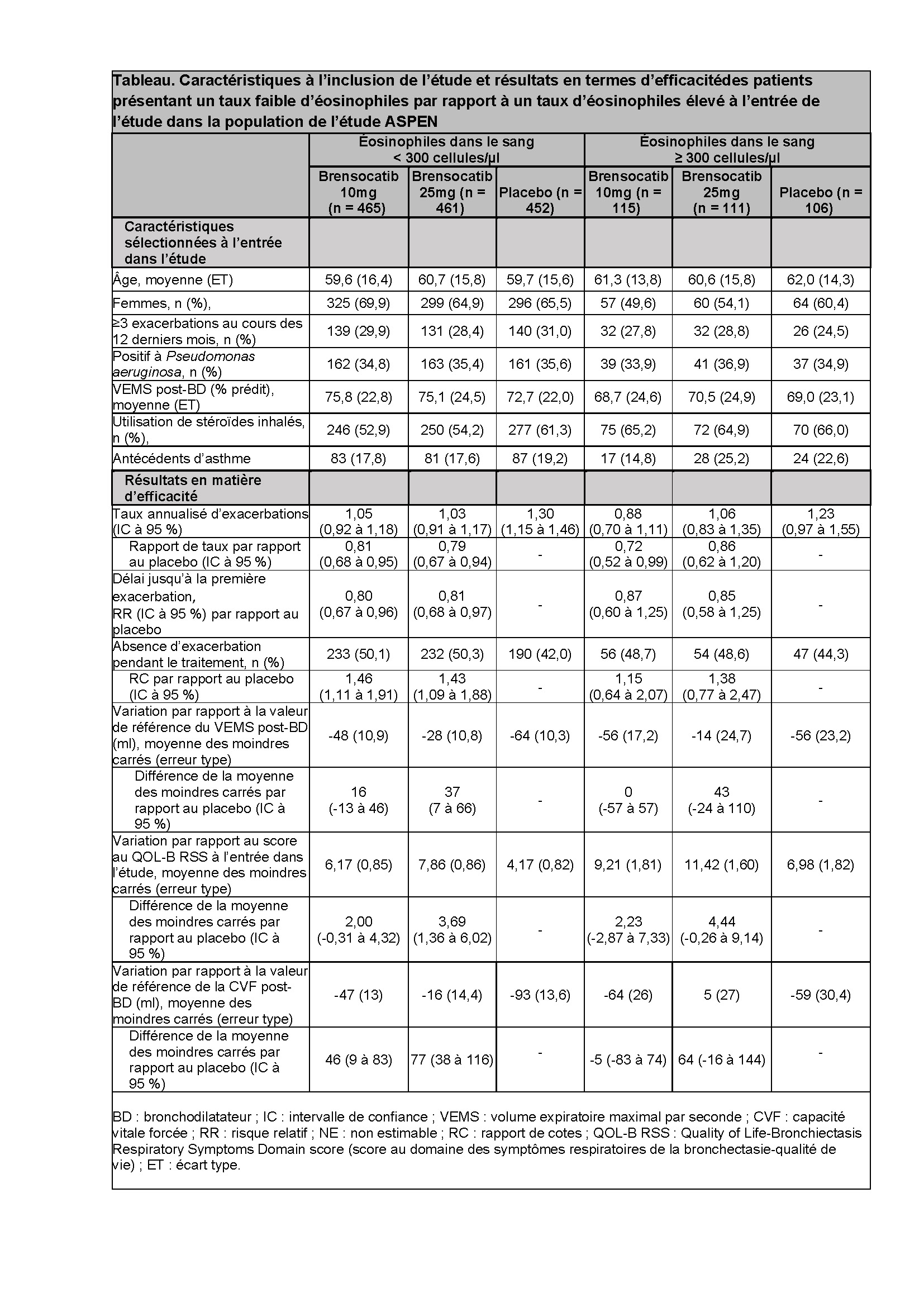
Les données démographiques et les caractéristiques à l’entrée de l’étude étaient comparables entre les sous-groupes (tableau). Conformément aux résultats globaux de l’étude ASPEN, le brensocatib, dosé à 10mg et à 25mg, a réduit le taux annualisé d’ExP, prolongé le délai jusqu’à la première ExP et a augmenté les chances de ne pas présenter d’ExP dans les deux sous-groupes (tableau). Le brensocatib 25mg a réduit le déclin du VEMS et de la CVF, et a amélioré le score QOL-B RSS à la semaine 52 par rapport au placebo dans les deux sous-groupes. Les événements indésirables étaient comparables entre les deux sous-groupes et cohérents avec les résultats globaux de l’étude.
Conclusion
Conformément à l’ensemble de la population de l’étude, les deux doses de brensocatib ont réduit le taux annualisé d’ExP, et le brensocatib à 25mg a réduit le déclin de la fonction pulmonaire et amélioré les symptômes chez des patients, indépendamment du taux d’éosinophiles à l’inclusion dans l’étude.
Burgel P-R. ; Chalmers J. ; Flume P. ; De Soyza A. ; Daley C. ; Fucile S. ; Shih V. ; Teper A. ; Shorb H. ; Mange K. ; Fernandez C.
