
Résumés CPLF 2026
Arrêt ou poursuitre des inhibiteurs de points de contrôle immunitaires à 2 ans de traitement pour les CBNPC de stade avancé: une analyse rétrospective des stratégies thérapeutiques de deux centres académiques
Auteur correspondant : De Gunten A.
Introduction
Chez les patients atteints d’un cancer bronchique non à petites cellules (CBNPC) avancé, la durée optimale du traitement par inhibiteurs de points de contrôle immunitaires (ICI) reste incertaine. Si certains essais de phase III limitent arbitrairement la durée de traitement à 2 ans, sa poursuite entraîne d'avantage de toxicités immuno-induites (irAE) et un surcoût financier. Les données sur l’arrêt systématique des ICI à 2 ans de traitement chez les patients contrôlés demeurent limitées.
Méthodes
Analyse rétrospective menée dans deux hôpitaux universitaires français entre 2015 et 2022 incluant des patients atteints de CBNPC avancé ayant reçu au moins 2 ans d’ICI. Le critère principal était la survie globale (OS). Les critères secondaires incluaient la survie sans progression (PFS), les examens d’imagerie réalisés à 2 ans et la décision thérapeutique à 2 ans associée.
Résultats
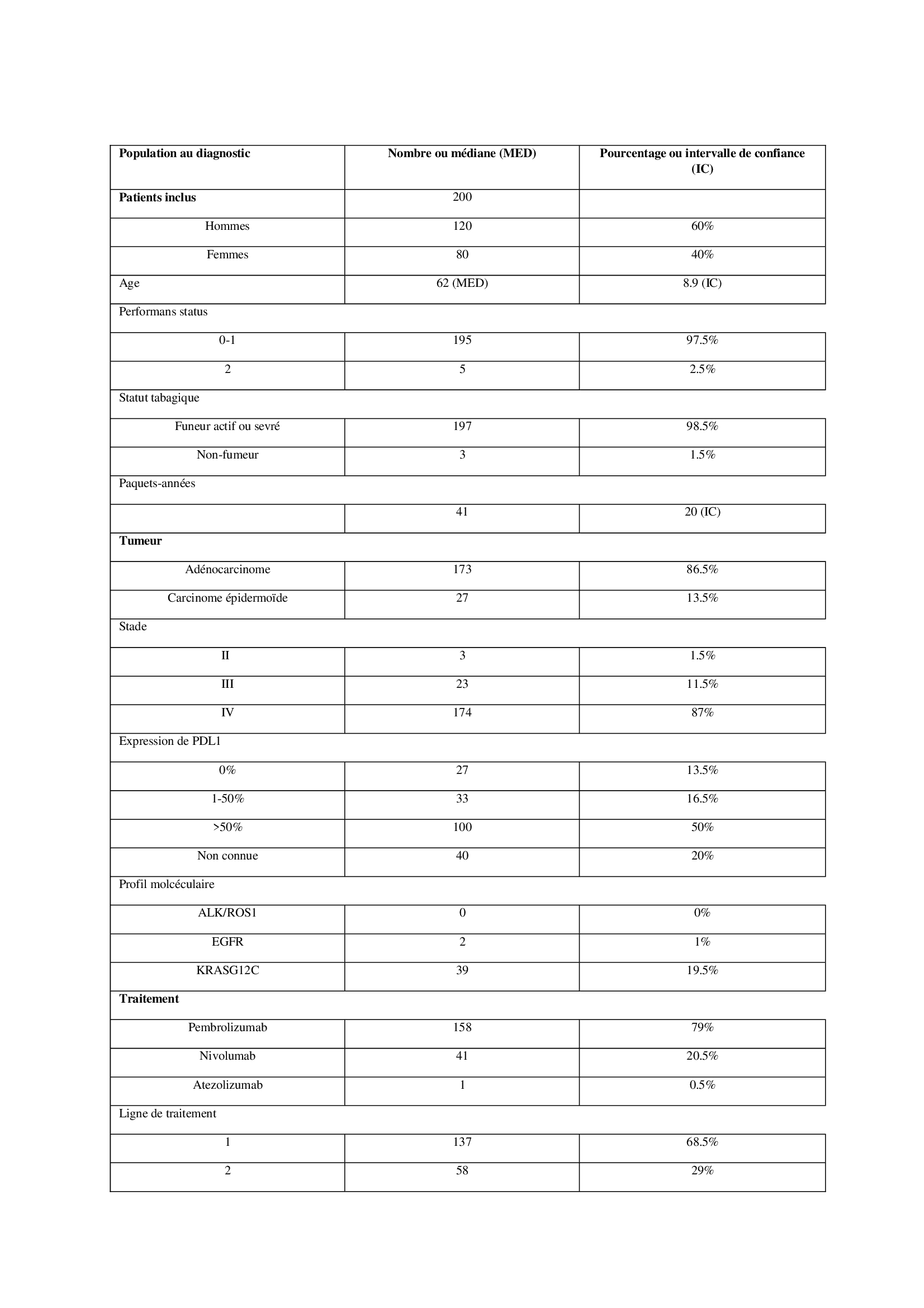
Deux cents patients ont été inclus : 49,5% ont interrompu le traitement et 50,5% l’ont poursuivi au delà de 2 ans. Les caractéristiques initiales étaient similaires entre les groupes. Les motifs de poursuite étaient : décision médicale (58,6%), demande du patient (10,1%), oligoprogression (10%), hypermétabolisme persistant (7,1%) et progression antérieure (6,1%). L’arrêt était associé à la présence d'irAE durant le traitement (OR 2,14 ; p < 0,05) et à la réponse tumorale (p < 0,01). Après un suivi médian de 45 mois, l’OS ne différait pas (non atteinte vs 86,8 mois ; p=0,87). La PFS non plus après 43 mois (74,1 vs 86,5 mois ; p=0,30). Après 2020, le recours au TEP augmentait (OR 6,2 ; p < 0,01) et était corrélé à un usage accru de traitements locaux (18,4% vs 6,2% ; p < 0,02).
Conclusion
L’arrêt du traitement par ICI à 2 ans chez les patients avec une maladie contrôlée à 2 ans n’altère pas la survie globale. Ces résultats rétrospectifs fournissent des données rassurantes pour la pratique clinique bien que de niveau de preuve limité.
Gunten (de) A. * ; Mogenet A. * ; Bronstein A. * ; Pollien E. * ; Floch (le) H. * ; Pluvy J. * ; Paleiron N. * ; Tomasini P. * ; Greillier L. * ; Bylicki O. *
*Déclarent ne pas avoir de lien d'intérêt en rapport avec ce résumé.
