
Résumés CPLF 2026
Amélioration rapide et soutenue du contrôle de l’asthme après l’initiation de tézépélumab chez des patients asthmatiques sévères non contrôlés : étude en vie réelle ASCENT
Auteur correspondant : Olivier C.
Introduction
Tézépélumab a démontré son efficacité chez les patients asthmatiques sévères non contrôlés dans les essais randomisés contrôlés. L'objectif de cette étude est d'évaluer le contrôle des symptômes en vie réelle chez les patients asthmatiques sévères non contrôlés après traitement par tézépélumab.
Méthodes
ASCENT (NCT05677139) est une étude prospective et observationnelle, actuellement en cours, menée chez des patients atteints d’asthme sévère non contrôlé en Europe et au Canada recevant tézépélumab conformément à la pratique clinique courante. Cette analyse intermédiaire a évalué la variation des scores ACQ-6 et SGRQ et du VEMS pré-bronchodilatateur (BD) entre l’inclusion et les semaines 4, 12 et 24 ainsi que du taux annuel d’exacerbation de l’asthme (TAEA) entre les 52 semaines avant l’inclusion et les 24 semaines de suivi.
Résultats
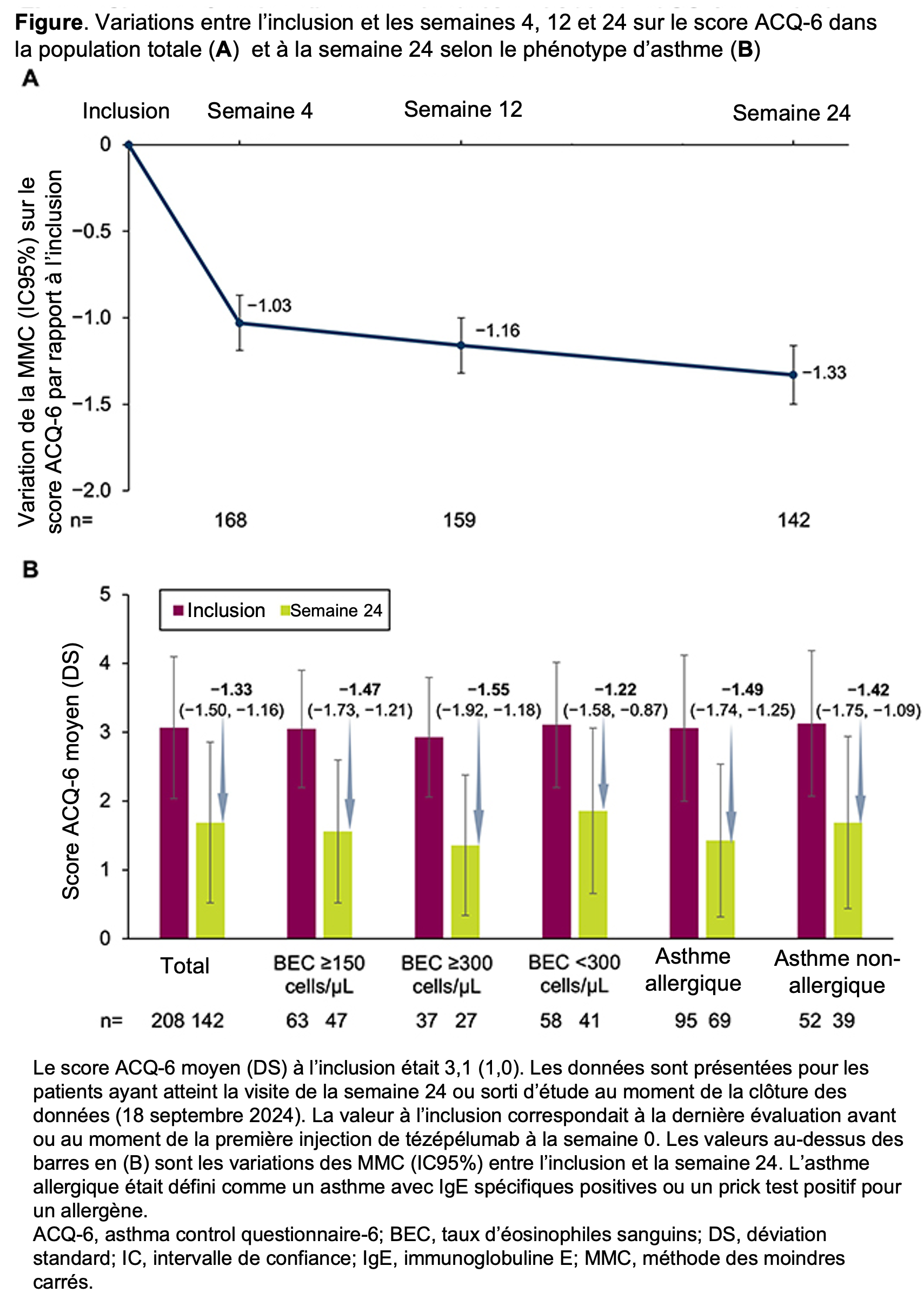
Au total, 211 patients ont été inclus. Les variations des moyennes des moindres carrés (MMC) du score ACQ-6 étaient de −1,03, −1,16 et −1,33 aux semaines 4, 12 et 24, respectivement, par rapport à l’inclusion. Ces diminutions ont été observées pour tous les phénotypes d’asthme (Figure). Des améliorations du score ACQ-6 atteignant ou dépassant le MCID étaient observées chez 64%, 71% et 78% des patients aux semaines 4, 12 et 24, respectivement. Les variations MMC de l’inclusion à la semaine 24 étaient de −19,79 pour le score SGRQ total et de 0,12 L pour le VEMS pré-BD. Le TAEA diminuait de 65% (IC95% : 55 ; 73).
Conclusion
Des améliorations cliniquement significatives du contrôle de l’asthme ont été observés avec le tézépélumab dès la semaine 4 et se sont maintenus jusqu’à la semaine 24, indépendamment du phénotype d’asthme, tout comme la fonction pulmonaire et les exacerbations.
Olivier C. a eu au cours des trois dernières années, une affiliation ou des intérêts financiers ou intérêts de tout ordre avec les sociétés commerciales suivantes : AstraZeneca, GSK, Novartis, Menarini, Sanofi ; Milger-Kneidinger K. a reçu des honoraires de conférencière et/ou pour sa participation à des advisory board de la part d’AstraZeneca, Chiesi, GSK, Novartis et Sanofi ; Dorscheid D. a reçu des subventions et du soutien pour les essais cliniques de la part d’AstraZeneca, association BC Lung, Instituts de recherche en santé du Canada, Michael Smith Health Research BC, Regeneron Pharmaceuticals, Sanofi et Teva Pharmaceuticals; et a reçu des honoraires de conférencier et de consulting, des subventions de déplacement, subventions de projets et des honoraires de rédaction de la part d’AstraZeneca, GSK, Novartis Canada, Regeneron Pharmaceuticals, Sanofi et Valeo Pharma ; Gessner C. a reçu des honoraires de conférencier ou pour du consulting de la part d’AstraZeneca, Berlin-Chemie, Boehringer Ingelheim, Bristol Myers Squibb, Chiesi, GSK, MSD, Novartis, Roche, Sanofi-Aventis et Teva Pharmaceuticals ; Hilberg O. a reçu des honoraires de conférencier et/ou pour sa participation à des advisory board de la part d’AstraZeneca, Chiesi, GSK et Sanofi ; Llanos JP. est un employé d’Amgen et possède des actions d’Amgen ; Nåtman J. est un employé d’AstraZeneca et peut détenir des actions ou des stock-options d’AstraZeneca ; Urbanski H. est un employé d’AstraZeneca et peut détenir des actions ou des stock-options d’AstraZeneca ; Clarke D. est un employé d’AstraZeneca et peut détenir des actions ou des stock-options d’AstraZeneca ; Emmanuel B. est un employé d’AstraZeneca et peut détenir des actions ou des stock-options d’AstraZeneca ; Stjepanovic N. est un employé d’AstraZeneca et peut détenir des actions ou des stock-options d’AstraZeneca
