
Résumés CPLF 2026
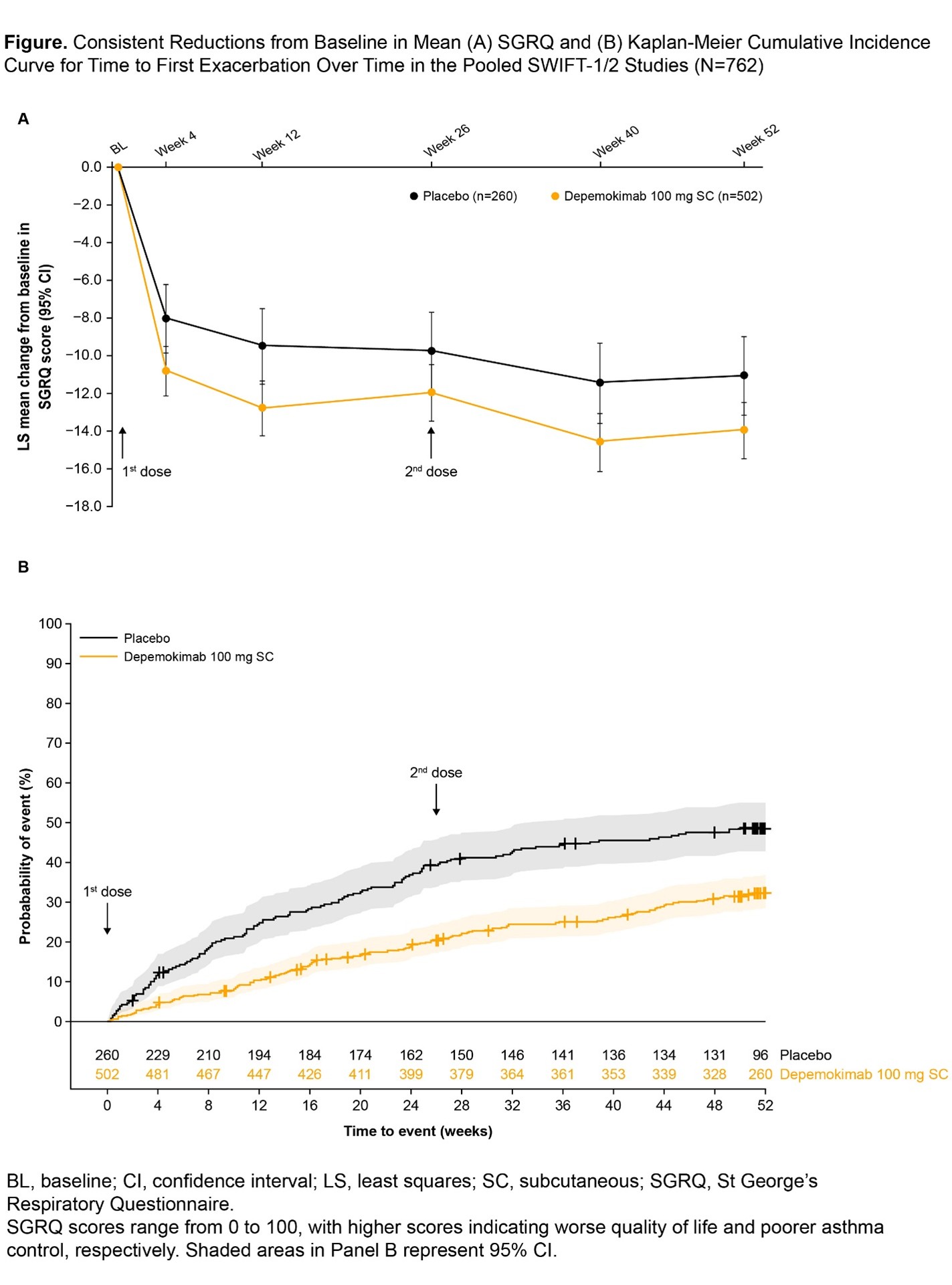
Efficacité soutenue du depemokimab au cours du temps dans l'asthme éosinophilique de type 2 : données regroupées des études de phase III SWIFT-1/2
Auteur correspondant : Picaud C.
Introduction
Depemokimab est le premier médicament biologique à longue durée d’action conçu avec une affinité de liaison à l'interleukine-5 améliorée, une puissance d'inhibition élevée et une demi-vie prolongée, permettant une administration deux fois par an chez les patients asthmatiques. Dans les études de phase III SWIFT-1/2, le traitement par depemokimab a significativement réduit le taux d'exacerbation annualisé de 54% avec une inhibition soutenue de l'inflammation de type 2 observée chez les patients atteints d'asthme éosinophilique de type 2 par rapport au placebo [1]. Le schéma posologique réduit de depemokimab pourrait alléger le fardeau du traitement ; ces analyses regroupées des études SWIFT-1/2 explorent comment l'efficacité de depemokimab est maintenue pendant l'intervalle posologique prolongé.
Méthodes
Des patients asthmatiques et présentant un nombre d'éosinophiles sanguins≥150 cellules/ μl lors du screening ou≥300 cellules/ μl au cours de l'année précédente ayant reçu des corticostéroïdes inhalés à dose moyenne à élevée ont été randomisés 2 : 1 pour recevoir depemokimab 100 mg par voie sous-cutanée ou un placebo toutes les 26 semaines pendant 52 semaines. Les patients étaient éligibles quel que soit leur score initial au questionnaire de contrôle de l'asthme (ACQ5). Les critères d'évaluation secondaires prédéfinis comprenaient le changement entre l’inclusion et la semaine 52 sur l'ensemble du questionnaire de St George (SGRQ) ; les autres critères d'évaluation prédéfinis comprenaient le délai avant la première exacerbation. Aucun ajustement de multiplicité n'a été effectué dans ces analyses groupées.
Résultats
Les populations de l'analyse complète pour les études SWIFT-1/2 comprenaient 762 patients (depemokimab, n=502 ; placebo, n=260). La variation moyenne (erreur-type) par rapport à l’inclusion du score SGRQ total était numériquement plus importante pour le depemokimab par rapport au placebo à la semaine 4 (-10,79 [0,669] vs -8,02 [0,928]) et s'est maintenue aux semaines 26 (-11,94 [0,763] vs -9,73 [1,054]) et 52 (-13,92 [0,758] vs -11,04 [1,055] ; Figure A). Cette observation était cohérente dans tous les domaines individuels, qui constituent le score total du SGRQ (les symptômes, l'activité et les impacts) et s'est maintenue au cours du temps. La probabilité de faire une exacerbation avec le depemokimab était plus faible qu'avec le placebo à la semaine 4. Cette différence s'est maintenue jusqu'à la semaine 52, et aucune augmentation du risque d'exacerbation n'a été observée dans les semaines précédant l'administration aux semaines 26 et 52 (Figure B). La probabilité de faire une exacerbation (intervalle de confiance [IC]) à 95% sur 52 semaines était de 32% (28%, 37%) avec le depemokimab et de 49% (43%, 55%) avec le placebo (hazard ratio [IC à 95%] 0,54 [0,43, 0,69]).
Conclusion
Le traitement par depemokimab administré deux fois par an a été associé à des bénéfices numériquement plus importants par rapport au placebo, maintenus pendant l'intervalle entre les doses, en termes de santé et de risque d'exacerbations chez les patients atteints d'asthme de type 2. Les résultats de cette analyse groupée des études SWIFT-1/2 soutiennent l'inhibition soutenue de l'inflammation de type 2 par depemokimab.
Financement : GSK (206713/213744 ; NCT04719832/NCT4718103). Poster initialement présenté à l’ATS, San Francisco, Etats-Unis, 18-21 mai 2025
Références
[1] Jackson DJ et al. NEJM 2024 ; 10,1056/NEJMoa2406673.
Wechsler ME. a reçu des honoraires de consultant, de conseil ou de conférencier d'Allakos, d'Amgen, d'Areteia Therapeutics, d'Arrowhead Pharmaceutical, d'AstraZeneca, d'Avalo Therapeutics, de Celldex, d'Eli Lilly, d'Equillium, de GSK, d'Incyte, de Kinaset, de Merck, de Phylaxis, de Pulmatrix, de Rapt Therapeutics, de recludix Pharma, de Regeneron, de Roche/Genentech, de Sanofi/Genzyme, de Sentien, de Sound Biologics, de Tetherex Pharmaceuticals, d'Uniquity Bio, d'Upstream Bio, de Verona Pharma et de Zurabio ; Panettieri RA. a reçu des subventions des NIH, de GSK, d'Origo Pharma et d'Astra Zeneca et des honoraires de consultation de Sanofi, Regeneron et AstraZeneca ; Muccino D. DM, RF, JK et AV sont des employés de GSK et détiennent des actions financières dans GSK ; Forth R. DM, RF, JK et AV sont des employés de GSK et détiennent des actions financières dans GSK ; Kwiatek J. DM, RF, JK et AV sont des employés de GSK et détiennent des actions financières dans GSK ; Vichiendilokkul A. DM, RF, JK et AV sont des employés de GSK et détiennent des actions financières dans GSK ; Jackson DavJ a reçu des honoraires de consultant/conférencier de GSK, AstraZeneca et Sanofi Regenero ; Picaud C. est un employé de GSK France et détient des actions financières de GSK
